Beskrivningar av goda svar: SV – Kemi
22.3.2024
Slutgiltiga beskrivningar av goda svar 14.5.2024
Grunderna enligt vilka bedömningen gjorts framkommer i de slutgiltiga beskrivningarna av goda svar. Uppgiften om hur bedömningsgrunderna tillämpats på examinandens provprestation utgörs av de poäng som examinanden fått för sin provprestation, de slutgiltiga beskrivningarna av goda svar och de föreskrifter gällande bedömningen som nämnden gett i sina föreskrifter och anvisningar. De slutgiltiga beskrivningarna av goda svar innehåller och beskriver inte nödvändigtvis alla godkända svarsalternativ eller alla godkända detaljer i ett godkänt svar. Eventuella bedömningsmarkeringar i provprestationerna anses vara jämställbara med anteckningar och sålunda ger de, eller avsaknaden av markeringar, inte direkta uppgifter om hur bedömningsgrunderna tillämpats på provprestationen.
Med studentexamensprovet utreds om studerandena tillägnat sig de kunskaper och färdigheter som anges i gymnasiets läroplan och uppnått tillräcklig mognad enligt målen för gymnasieutbildningen. Målet för bedömningen i läroämnet kemi är en förståelse för och en tillämpning av den kemiska kunskapen. Vid bedömningen beaktas även de färdigheter med vilka man tillägnar sig experimentell kunskap och förmågan att behandla den. Till sådan kunskap hör till exempel planering av experiment, trygg hantering av arbetsredskap och reagens, presentation och tolkning av resultat samt förmågan att dra slutsatser och tillämpa dem.
Vid bedömningen av uppgifterna i kemi läggs vikten vid ett framställningssätt som betonar läroämnets karaktär och vid precision i begreppen och språkbruket. Reaktionsformlerna ställs upp utan oxidationstal med minsta möjliga heltalskoefficienter och med aggregationstillstånden angivna. I organiska reaktionslikheter används strukturformler, men aggregationstillstånd krävs inte. Olika sätt att skriva strukturformler godkänns.
I beräkningsuppgifter ska storhetsekvationer och formler användas på ett sätt som visar att examinanden förstått uppgiften rätt och tillämpat korrekt princip eller lag i sin lösning. Av svaret framgår entydigt hur man når slutresultatet, men omfattande mellansteg behövs inte. CAS-program kan utnyttjas i uppgiftens olika skeden. De principer och lagar som gäller den aktuella situationen samt uppgiftens slutresultat och de slutsatser som dras utgående från lösningen är av central betydelse och ska framgå av svaret. Slutresultaten ges med enheter och med den noggrannhet som utgångsvärdena kräver, och slutsatserna motiveras.
Mätresultat och grafer som ritats utgående från dessa utnyttjas vid analysen av data och då man drar slutsatser. Till mätpunkterna anpassas en vederbörlig rät linje. Värden som ligger mellan mätpunkterna kan interpoleras med ögonmått genom visuell avläsning av grafen eller med hjälp av ett lämpligt program. Axlarnas namn, enheter och skala märks ut i grafen. I grafen anges sådana punkter som är väsentliga för slutsatserna, som ekvivalenspunkten för en titrerkurva eller tangenten som används när man beräknar en hastighet vid en given tidpunkt.
I essäsvar och förklarande svar kompletteras texten med reaktionsformler, ekvationer eller teckningar. Fenomenen som behandlas beskrivs på makroskopisk, mikroskopisk och symbolisk nivå. Av svaret framgår att det material som hör ihop med uppgiften har använts, tillämpats, analyserats och utvärderats i enlighet med uppgiftsformuleringen. Ett svar på god nivå är välstrukturerat och innehållsmässigt konsekvent.
Svaren bedöms enligt de kriterier som gäller för respektive uppgift. Utgångspunkten vid bedömningen är de förtjänster för vilka poäng ansamlas. Om en central kemisk princip saknas eller är felaktig avslutas poängansamlingen. Då godkänns inte fortplantning av det felaktiga resultatet (ej-FF). Exempel på sådana fel är stökiometrifel, fel begränsande faktor samt fel ämne i en reaktionslikhet. För övriga brister eller fel godkänns fortplantning av det felaktiga resultatet (FF), och då fortsätter ansamlingen av poäng efter bristfälligheten eller felet. I de krävande uppgifterna i provets del 3 förutsätts en större precision i behandlingen av principer än i de grundläggande uppgifterna i början av provet. Ur kemisk synvinkel inexakt språkbruk, små räknefel eller slarvig användning av närmevärden orsakar avdrag på 0–3 p. till exempel på följande sätt:
- avrundnings- och kopieringsfel som inte påverkar slutresultatet, −0 p.
- kopieringsfel, avrundningsfel och små slarvfel som påverkar slutresultatet, ett enskilt litet fel i en strukturformel, −1 p.
- enhetsomvandlingsfel, systematiska fel i en strukturformel samt övriga fel som till sin natur är allvarligare än små fel, men där det ändå inte är fråga om en felaktig kemisk princip, −2 p.
4.6.2024 kl. 11.30 korrigerat poängsättningen för totalreaktionen i deluppgift 9.3.
Del 1: 20-poängsuppgift
1. Flervalsuppgifter från kemins olika delområden 20 p.
1.1 Vilket av följande ämnen är till sitt aggregationstillstånd en gas vid rumstemperatur? 2 p.
- kolmonoxid (2 p.)
1.2 Vilket av följande ämnen har den största elektronegativiteten? 2 p.
- F (2 p.)
1.3 Vilket salt ger upphov till en sur vattenlösning? 2 p.
- NH₄Cl (2 p.)
1.4 Vad sker i reaktionen 2CuSO₄ + 4KI → 2CuI + I₂ + 2K₂SO₄? 2 p.
- Jod oxideras och koppar reduceras. (2 p.)
1.5 Vilken förening bildas, förutom vatten, då butanol och ättiksyra reagerar? 2 p.
- butyletanat (2 p.)
1.6 Volymen för ett idealgasprov på en mol fördubblas medan temperaturen hålls oförändrad. Följden är att gasprovets tryck 2 p.
- halveras. (2 p.)
1.7 Vilket av följande metallpar ger upphov till den största cellspänningen? 2 p.
- Ni och Mg (2 p.)
1.8 Vilken av följande kombinationer skulle kunna fungera som en buffertlösning? 2 p.
- NH₃(aq) och NH₄Cl(aq) (2 p.)
1.9 Man kan separera ämnen som är lösta i varandra med hjälp av destillering. Destillering utgår från skillnader i ämnenas 2 p.
- kokpunkter. (2 p.)
1.10 Mellan molekylerna i kvävgas förekommer 2 p.
- dispersionskrafter. (2 p.)
Del 2: 15-poängsuppgifter
2. Framställning av väte och väte som bränsle 15 p.
2.1 Väte framställdes ur vatten i ett elektrolysexperiment. Under experimentet reagerade 300,0 g vatten. Gaserna som bildades samlades in. Hur stor volym hade vätgasen och hur stor volym hade syrgasen som bildades? Båda gaserna hade trycket 101,325 kPa och temperaturen 293,15 K. 8 p.
n(H₂O) = m / M = 300,0 g / 18,016 g/mol = 16,6519 mol
(1 p.)
Utifrån reaktionsformeln 2 H₂O(l) → 2 H₂(g) + O₂(g)
(1 p.)
får vi
n(H₂) = n(H₂O) = 16,6519 mol
(1 p.)
n(O₂) = ½ · n(H₂O) = ½ · 16,6519 mol = 8,325 95 mol
(1 p.)
- om stökiometrin är felaktig eller något annat principfel görs vid beräkningen av substansmängden ansamlas inte poäng från beräkningen av volymen för ifrågavarande gas (ej-FF).
V(H₂) = n(H₂) · RT/p = 16,1659 mol · 8,314 46 Pa · m³ / (mol · K) · 293,15 K / (101 325 Pa)
V(H₂) = 0,4005624 m³ ≈ 0,4006 m³ = 400,6 l
(2 p.)
V(O₂) = n(O₂) · RT/p = 8,32595 mol · 8,314 46 Pa · m³ / (mol · K) · 293,15 K / (101 325 Pa)
V(O₂) = 0,2002812 m³ ≈ 0,2003 m³ = 200,3 l
(2 p.)
- Fel i enhetsomvandlingarna, −2 p. avdrag för deluppgiften
- Små räknefel såsom felslag och avrundningsfel, −1 p./fel
- Svarets siffernoggrannhet motsvarar inte uppgiften, −1 p. avdrag för deluppgiften
- I uppgiften kan man också använda molvolymens värde Vₘ = 24,055 dm³/mol eftersom det motsvarar förhållandena (p, T) i uppgiften. Om fel värde för molvolymen används blir det 0 p. för uträkningarna av volymerna.
2.2 Då man framställer väte genom elektrolys av vatten i ett laboratorium använder man ofta inte rent vatten. Istället använder man vatten som innehåller upplöst natriumsulfat eller något annat upplöst salt. Förklara varför man gör så. 3 p.
Rent vatten leder elektricitet dåligt,
ELLER Tillsatsen av salt förbättrar konduktiviteten / gör elektrolysen mer effektiv / försnabbar reaktionen. (1 p.)
- Godkänns inte om saltet påstås vara en katalysator.
eftersom det innehåller en mycket liten mängd laddningstransportörer. I vattenlösningen har natriumsulfatet (eller något annat salt) dissocierat till joner med negativ och positiv laddning. (1 p.)
- Ur svaret måste dissociationen till joner framgå.
De här jonerna kan transportera laddning i lösningen, (1 p.) (och därför ökar den elektriska ledningsförmågan. Då elledningsförmågan blir större kommer elströmmen som behövs för elektrolysreaktionen lättare att ledas genom vattenlösningen.)
2.3 Då man använder väte som trafikbränsle produceras elektricitet ur vätet med hjälp av en bränslecell i bilen. Den producerade elektriciteten driver bilens elmotor. Beskriv en fördel och en nackdel med användningen av väte som trafikbränsle. 4 p.
En fördel har nämnts, 1 p. och preciserats, 1 p. (Enbart en fördel och dess precisering beaktas i poängsättningen).
- Fördel: Vid användningen bildas vatten. / Väte är miljövänligt att använda.
Precisering: Det bildas enbart vatten ELLER Det bildas inte några växthusgaser / luftföroreningar / skadliga ämnen. - Fördel: Vid framställningen av väte bildas inga växthusgaser
Precisering: om elektriciteten som behövs för elektrolys av vatten är producerad med förnybar energi. - Fördel: Vätets energiinnehåll är stort
Precisering: per massenhet. - Fördel: Det går snabbt att tanka väte
Precisering: jämfört med att ladda en elbil. - Fördel: Bränslecellen har en bra effekt
Precisering: även vid kallt väder. - Fördel: Då man använder väte kan man ersätta fossila bränslen
Precisering: som inte är förnybara naturresurser / som ger upphov till växthusgaser.
En nackdel har nämnts, 1 p. och preciserats, 1 p. (Enbart en nackdel och dess precisering beaktas i poängsättningen).
- Nackdel: Det är krångligt att lagra / transportera väte
Precisering: för vätet är mycket reaktivt / läcker lätt genom olika material ELLER då det kräver högt tryck / låg temperatur ELLER för väte har en låg kokpunkt. - Nackdel: Väte är explosivt / brandfarligt
Precisering: om vätet reagerar med syre / luften. - Nackdel: Vätets energiinnehåll är litet
Precisering: per volymenhet. - Nackdel: Framställningen av väte ger upphov till koldioxidutsläpp
Precisering: om vätet framställs ur fossila bränslen / om man använder elektricitet som producerats med fossila bränslen. - Nackdel: Förbrukningen av elektricitet / energi ökar
Precisering: eftersom framställningen av väte kräver en stor mängd energi / elektricitet. - Nackdel: Det är inte möjligt att tanka vätgas
Precisering: för det finns inte ännu något distributionsnät.
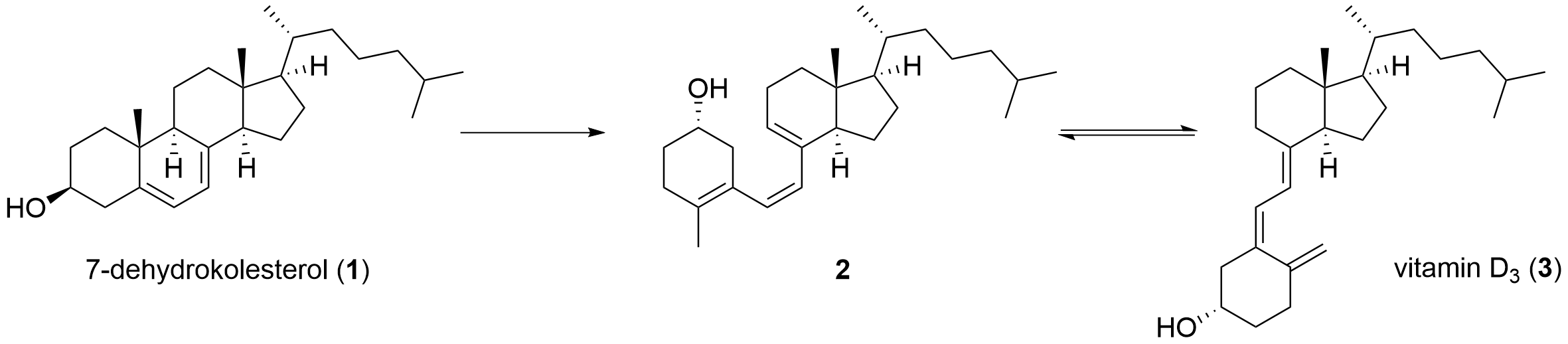
3. Vitamin D₃ 15 p.
Bildandet av vitamin D₃ (3) ur 7-dehydrokolesterol (1) kan beskrivas med reaktionsformeln nedan.
Då huden utsätts för solljus bildas vitamin D₃ (3) på huden utgående från 7-dehydrokolesterol (1). Under inverkan av UV-B-strålning med hög energi bildas först förening 2 av 7-dehydrokolesterolet (1). Sedan isomereras förening 2 till vitamin D₃ (3). Reaktionen mellan föreningen 2 och vitamin D₃ (3) är en jämviktsreaktion vars jämviktskonstants värde beror på hudens temperatur.
Du kan utnyttja material och i deluppgifterna.
3.1 Är 7-dehydrokolesterol (1) och förening 2 isomerer sinsemellan? Motivera ditt svar. 3 p.
Föreningarna är isomerer sinsemellan (1 p.) eftersom de har samma molekylformel (1 p.).
Molekylformeln för 7-dehydrokolesterol (1) är C₂₇H₄₄O och molekylformeln för förening 2 är också C₂₇H₄₄O
(1 p.) (, så de är isomerer).
3.2 Hör vitamin D₃ (3) till de vattenlösliga eller de fettlösliga vitaminerna? Motivera ditt svar. 4 p.
Vitamin D3 består av en opolär kolvätestam (1 p.) och den innehåller bara en polär grupp, en hydroxigrupp (1 p.) (, som kan bilda vätebindningar med vatten).
De opolära delarna av molekylen är förhållandevis stora, och därför har en enskild hydroxigrupp bara en liten inverkan på lösligheten.
(1 p.)
Vitamin D3 (löser sig därmed bättre i opolära föreningar än i vatten och) hör därför till de fettlösliga vitaminerna.
(1 p.)
- Sådana felaktigheter som upphäver en förtjänst i svaret leder till att ifrågavarande poäng förloras.
3.3 Utgående från en studie vet vi att jämviktskonstanten (K) för isomeriseringsreaktionen mellan förening 2 och vitamin D₃ (3) har värdet 11,4 vid temperaturen som råder på en människas hud. Då reaktionen har nått jämvikt har det bildats en blandning som innehåller både vitamin D₃ (3) och förening 2. Hur många procent av den här blandningen utgörs av vitamin D₃ (3)? 8 p.
Vi skriver uttrycket för jämviktskonstanten: K = [D₃] / [2] = 11,4.
(1 p.)
- Om jämviktskonstantens uttryck är felaktigt avslutas poängansamlingen (ej-FF), 0 p. för deluppgiften.
Den sammanlagda koncentrationen av förening 2 och vitamin D₃ på huden är: c(tot.) = c(2) + c(D₃)
(1 p.)
- Om uppgiften har lösts enbart med substansmängder måste en motivering till att volymerna förkortas bort i uttrycket för jämviktskonstanten framgå ur svaret. Annars avdras −2 p.
I utgångsläget har det ännu inte bildats någon vitamin D₃, och därför gäller c(2, början) = c(tot.).
Vi gör upp en jämviktstabell:
| Förening 2 | D₃ | |
|---|---|---|
| I början | c(tot.) | 0 |
| Vid jämvikt | c(tot.) – x | x |
(2 p.)
Vi sätter in jämviktskoncentrationerna i uttrycket för jämviktskonstanten:
K = [D₃] / [2]
x / (c(tot.) – x) = 11,4
(1 p.)
x = 11,4 ∙ c(tot.) – 11,4 ∙ x
12,4 ∙ x = 11,4 ∙ c(tot.)
x = 11,4 ∙ c(tot.) / 12,4
Andelen vitamin D₃ av den totala mängden:
c(D₃) / c(tot.) = x / c(tot.)
(1 p.)
= 11,4 ∙ c(tot.) / (12,4 ∙ c(tot.)) = 11,4 / 12,4 = 0,91935 ≈ 91,9 %
(2 p.)
- Ur svaret ska det framgå att jämviktssituationen har gestaltats på rätt sätt.
4. Titrering 15 p.
4.1 Vilka redskap behöver du för titreringen? Förklara steg för steg hur titreringen utförs i praktiken. Hur identifieras ekvivalenspunkten? 11 p.
Följande redskap behövs för att utföra titreringen:
(1 p./redskap, högst 3 p.)
- Byrett
- Vollpipett (fyllpipett)/mätpipett/mätglas(, för att mäta upp ättiksyralösningen noggrant.)
- pH-mätare / pH-elektrod / indikatorlösning
Därtill ansamlas högst 1 p. för följande redskap (ett redskap räcker)
- Dekanterglas eller motsvarande kärl (,som innehåller reagenset vars koncentration ska bestämmas.)
- Stativ (och klämmor)
- Magnetomrörare / glasstav / något annat redskap som kan användas för omrörning
I svaret beskrivs hur titreringen utförs.
(1 p./moment, högst 6 p.)
- En viss volym av ättiksyran mäts upp noggrant / med ett noggrant mätredskap och sätts i dekanterglaset.
- Natriumhydroxidlösning sätts i byretten.
- Natriumhydroxiden (vars koncentration är känd) tillsätts lite i taget / droppvis från byretten
- Natriumhydroxiden tillsätts till ättiksyran (som är i dekanterglaset).
- Förbrukningen antecknas under arbetets gång (man för laboratoriedagbok/protokoll).
- Avläsning av byrettens skala: den böjda ytans lägsta punkt ska vara vid strecket på byretten.
- Lösningen rörs om / magnetomröraren är påslagen hela tiden.
I svaret förklaras hur ekvivalenspunkten identifieras. (2 p.)
- Förklaring med hjälp av en indikator: Titreringen avslutas då färgen har förändrats (1 p.). Färgförändringen är bestående. (1 p.)
ELLER
- Förklaring med hjälp av pH-mätare: Man mäter pH-värdet (1 p.) tills ekvivalenspunkten har passerats, och ekvivalenspunkten bestäms vid mitten av den kraftigaste stigningen på titrerkurvan / med hjälp av derivatan (1 p.).
- Om inte titrering har beskrivits i svaret, 0 p. för deluppgiften.
- Om titreringen inte är en neutraliseringstitrering kan högst 2 p. ansamlas för deluppgiften. De här poängen ansamlas från beskrivningen av utförandet om NaOH och ättiksyran är i rätt kärl/redskap i början.
4.2 Är lösningen vid titreringens ekvivalenspunkt sur, neutral eller basisk? Vilken är en bättre indikator för den här titreringen: metylröd eller fenolftalein? Motivera ditt svar utan beräkningar. 4 p.
Lösningen är basisk vid ekvivalenspunkten (1 p.) eftersom man titrerar en svag syra med en stark bas / eftersom det finns acetatjoner i lösningen vid ekvivalenspunkten och acetatjonen är en svag bas (1 p.).
Fenolftalein är lämplig som indikator (1 p.), eftersom färgförändringen för fenolftalein sker vid pH-värdet 8,3–10,0 / vid ett basiskt pH-värde (1 p.).
- De två sista poängen ansamlas bara om lösningens basiskhet framgår ur svaret.
5. Videor av reaktioner och att skriva reaktionsformler 15 p.
5.1 Se videon . En bit av ett magnesiumband läggs i en vätekloridsyralösning. Vilka observationer gör du gällande reaktionen? Skriv reaktionsformeln (reaktionslikheten). 5 p.
Observationer:
Det bildas gasbubblor i reaktionen. (1 p.)
Magnesiumbandet fräts eller löser sig. (1 p.)
- Poängen för observationerna ansamlas inte om processen har tolkats på ett ur kemisk synvinkel felaktigt sätt (till exempel lösningen kokar, det bildas syre eller magnesium smälter).
Reaktionsformel:
2HCl (aq) + Mg (s) → H₂ (g) + MgCl₂ (aq)
Utgångsämnen och reaktionsprodukter (1 p.), koefficienterna (1 p.), aggregationstillstånden (1 p.)
- Poängen för koefficienterna och aggregationstillstånden kan ansamlas bara om ämnena är rätt.
5.2 Se videon . Kaliumjodid tillsätts i en vattenlösning av väteperoxid. Kaliumjodiden katalyserar reaktionen. Vilka observationer gör du gällande reaktionen? Skriv reaktionsformeln. Du behöver inte skriva ut katalysatorn i reaktionsformeln. 5 p.
Observationer:
Det bildas gasbubblor i reaktionen. (1 p.)
Lösningens färg förändras (och blir gul). (1 p.)
- Poängen för observationerna ansamlas inte om processen har tolkats på ett ur kemisk synvinkel felaktigt sätt (till exempel lösningen kokar eller det bildas väte).
Reaktionsformel:
2H₂O₂ (aq) → 2H₂O (l/aq) + O₂ (g)
Utgångsämnen och reaktionsprodukter (1 p.), koefficienterna (1 p.), aggregationstillstånden (1 p.)
- Poängen för koefficienterna och aggregationstillstånden kan ansamlas bara om ämnena är rätt.
5.3 Se videon . Kaliumpermanganatlösning tillsätts i en sur järn(II)sulfatlösning. Vilka observationer gör du gällande reaktionen? Skriv reaktionsformeln. 5 p.
Observationer:
(Kaliumpermanganatlösningens violetta) färg försvinner. (1 p.)
Reaktionsformel:
5Fe²⁺ (aq) + MnO₄⁻ (aq) + 8H⁺ (aq) → 5Fe³⁺ (aq) + Mn²⁺ (aq) + 4H₂O (l)
ELLER
5Fe²⁺(aq) + MnO₄⁻ (aq) + 8H₃O⁺ (aq) → 5Fe³⁺ (aq) + Mn²⁺ (aq) + 12H₂O (l)
Poängsättning:
- Ur reaktionen framgår oxidationen: Fe2+ → Fe3+, 1 p.
- Ur reaktionen framgår reduktionen: Mn7+ → Mn2+, 1 p.
- Alla ämnen och koefficienter i totalreaktionen är rätt, 1 p.
- Alla aggregationstillstånd i totalreaktionen är rätt, 1 p. (förutsätter att de föregående tre poängen har ansamlats).
6. Strukturerna för atomer och kärnor 15 p.
1 p. för varje korrekt ord eller tal.
Då svaret är ett tal godkänns också samma tal skrivet med bokstäver. Synonymer som ur kemisk synvinkel är korrekta godkänns.
6.1 1 p.
- 9 (1 p.)
6.2 1 p.
- 7 (1 p.)
6.3 1 p.
- 1 (1 p.)
6.4 1 p.
- neon (1 p.)
6.5 1 p.
- reduktion (1 p.)
6.6 1 p.
- kovalenta (1 p.)
6.7 1 p.
- +6 (1 p.)
- +VI (1 p.)
6.8 1 p.
- +6 (1 p.)
- +VI (1 p.)
6.9 1 p.
- 80 (1 p.)
6.10 1 p.
- +4 (1 p.)
- +IV (1 p.)
6.11 1 p.
- 92 (1 p.)
6.12 1 p.
- 143 (1 p.)
6.13 1 p.
- plutonium (1 p.)
- Pu (1 p.)
6.14 1 p.
- 239 (1 p.)
6.15 1 p.
- 94 (1 p.)
Även andra korrekta uttryck godkänns.
7. Återvinning av förpackningsmaterial 15 p.
7.1 Läskedrycker och livsmedel förpackas ofta i burkar tillverkade av aluminium. De är lätta och tåliga mot korrosion. Förklara vad den goda korrosionsbeständigheten hos aluminium beror på. 2 p.
Då aluminium reagerar med syret ur luften bildas det snabbt ett lager av aluminiumoxid på aluminiumets yta. (1 p.) Det skyddar aluminiumet från att ytterligare oxideras. (1 p.)
Den senare poängen förutsätter att något skyddande lager har identifierats och att en kemisk motivering till korrosionståligheten har angivits. Till exempel:
- det skyddande lagret är kemiskt stabilt
- det skyddande lagret är hårt/tätt
- det skyddande lagret bildas snabbt
- det skyddande lagret fungerar som en elektrisk isolator
7.2 En stor del av aluminiumet i förpackningar kan återvinnas. Diskutera orsaker till att aluminium har en hög återvinningsgrad. 4 p.
Till exempel följande orsaker kan diskuteras i svaret:
- Aluminium i ren form förekommer inte i naturen (1 p.), men genom återvinning erhåller man aluminium som är nästan rent för vidare förädling. (1 p.) Det här förbrukar mindre energi och är därför ekonomiskt lönsamt. (1 p.)
- Den kemiska strukturen för aluminium förändras / aluminiumets kvalitet försämras inte inte under återvinningsprocessen. (1 p.)
- Aluminium är lätt att omforma. (1 p.)
- Pantsystemet för läskedrycksburkar uppmuntrar till att återvinna burkarna. (1 p.) Det finns insamlingspunkter för aluminium/metall på många ställen (1 p.). Det är förmånligt att transportera aluminium eftersom den är lätt (1 p.)
7.3 Fiberförpackningar tillverkade av papper och kartong är det vanligaste förpackningsmaterialet i Finland. Papper och kartong består huvudsakligen av cellulosafibrer. Beskriv den kemiska strukturen för cellulosa. Vilka är de starkaste bindningarna mellan cellulosamolekylerna? 4 p.
I cellulosafibrerna är vätebindningen den starkaste bindningen mellan cellulosakedjorna. (1 p.)
- Om en felaktig bindning dessutom har nämnts, 0 p.
Beskrivning av strukturen för cellulosapolymeren och -fibern, högst 2 p.:
- Cellulosa består av glukosmonomerer (1 p.).
- Cellulosa är en polymer/polysackarid/kolhydrat/makromolekyl/molekyl med lång kedja. / Cellulosa innehåller hydroxigrupper. (1 p.)
Ytterligare högst 1 p. kan fås av följande (en observation är tillräckligt):
- Kedjan är linjär (på grund av glykosidbindningarnas konformation). (1 p.)
- Det kan bildas flera vätebindningar. (1 p.)
- Mellan monomererna finns det en glykosidbindning / syrebrygga. (1 p.)
7.4 Plaster är populära förpackningsmaterial för att de är lätta, hållbara och förmånliga. Återvinningsgraden för olika plastsorter varierar stort. Diskutera vilka orsaker som gör det svårt att återvinna plaster. Förklara varför vissa plaster lämpar sig bättre och andra plaster lämpar sig sämre för återvinning. 5 p.
Faktorer som försvårar återvinningen av plaster (högst 3 p.):
Till exempel (1 p./faktor):
- Plasternas kemiska mångfald försvårar sorteringen / återanvändningen.
- I många konsumentprodukter har man kombinerat olika plastsorter med varandra / med andra material, så det är krångligt / dyrt att separera dem från varandra.
- Tillsatsämnen (mjukgörare / stabiliseringsämnen / färgämnen) inverkar på hur plasten måste behandlas och hur väl den kan återanvändas.
- Smutsiga plaster leder till att rena plastpartier kan kontamineras och det sänker kvaliteten på slutprodukten / leder till att återanvändningen inte är ekonomiskt lönsam.
- Det är förmånligt att tillverka plast / plastens råämnen har ett lågt värde så återanvändningen är inte alltid ekonomiskt lönsam.
- Det är lätt att förbränna plast / använda plast till att producera energi och det minskar på återanvändningen.
- Det är långa avstånd mellan insamlingskärlen för plast (exempelvis på glesbygden) / Det saknas ett retursystem för plastförpackningar som bygger på pant.
Orsaker till att vissa plaster är bättre lämpade för återvinning än andra (högst 2 p.):
Till exempel (1 p./faktor):
- En enkel kemisk struktur / sammansättning hos polymeren underlättar återanvändningen.
- Termoplaster kan omformas genom upphettning, men inte härdplaster.
- I termoplaster är bindningarna mellan polymerkedjorna svaga, i härdplasterna är de starkare.
- Vissa plaster / tillsatsämnen kan frigöra giftiga ämnen under återanvändningsprocessen (till exempel PVC).
8. Framställningsreaktionen för ett doftämne i parfymer 15 p.
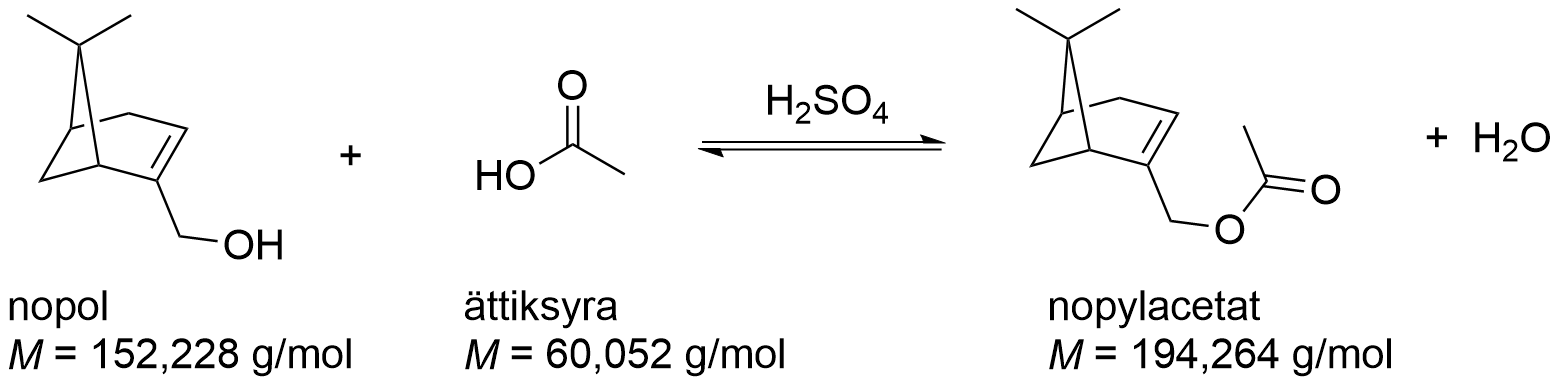
Nopylacetat är ett ämne som har en fruktig och träig doft och som används i parfymer. Nopylacetat kan framställas till exempel med förestringsreaktionen mellan nopol och ättiksyra, som visas i bilden. Molmassorna för utgångsämnena och produkterna visas också i bilden. Använd dem då du löser uppgiften.
I ett visst experiment framställde man nopylacetat med en förestringsreaktion genom att lösa upp nopol i ättiksyra. Massan för nopol var 20,0 g och för ättiksyra 15,8 g. Svavelsyra tillsattes som katalysator i reaktionsblandningen och blandningen upphettades till temperaturen 50 °C. Reaktionsblandningens totalvolym var då 26,4 ml.
8.1 Då jämvikt hade uppnåtts isolerade man nopylacetatet. Massan för det rena och isolerade nopylacetatet var 15,1 g. Vilket var det procentuella utbytet av nopylacetat? 7 p.
n(nopol) = m / M = 20,0 g / 152,228 g/mol = 0,13138 mol
n(ättiksyra) = 15,8 g / 60,052 g/mol = 0,26311 mol
(3 p.)
Poängsättning: ena substansmängden rätt, 2 p., båda rätt, 3 p.
Bestämning av den begränsande faktorn:
Utifrån de stökiometriska koefficienterna reagerar nopol och ättiksyra med varandra i substansmängdsförhållandet 1:1. (1 p.) Därmed finns ättiksyra i överskott och nopol är den begränsande faktorn. (1 p.)
- Om fel begränsande faktor har valts tar poängansamlingen slut (ej-FF).
- Om den begränsande faktorn inte har motiverats men beräkningen fortsätter utifrån rätt ämne erhålls inte poängen för bestämning av den begränsande faktorn men poängansamlingen fortsätter (FF).
Då får vi n(nopol) = n(nopylacetat).
Det teoretiska utbytet av nopylacetat:
m(nopylacetat) = n(nopylacetat) · M(nopylacetat)
= 0,13138 mol · 194,264 g/mol = 25,523 g
(1 p.)
Det procentuella utbytet: 15,1 g / 25,523 g = 0,5916 \approx 59,2 %.
(1 p.)
Svar: Det procentuella utbytet av nopylacetat är 59,2 %.
8.2 Reaktionens jämviktskonstant är 2,90 vid temperaturen 50 °C. Beräkna jämviktskoncentrationerna för alla föreningar. 8 p.
c = n / V och n = m / M.
Då vi kombinerar de här ekvationerna får vi: c = m / (M · V).
c(nopol) = m / (M · V) = 20,0 g / (152,228 g/mol · 0,0264 dm³) = 4,9766 mol/l
(1 p.)
c(ättiksyra) = m / (M · V) = 15,8 g / (60,052 g/mol · 0,0264 dm³) = 9,9661 mol/l
(1 p.)
K=\frac{\mathrm{[nopylacetat]\cdot[vatten]}}{\mathrm{[nopol]\cdot[ättiksyra]}}
(1 p.)
Vi betraktar jämvikten:
| nopol | + | ättiksyra | ⇌ | nopylacetat | vatten | |
| cbörjan (mol/l) | 4,9767 | 9,9661 | 0 | 0 | ||
| cjämvikt (mol/l) | 4,9767–x | 9,9661–x | x | x |
(2 p.)
- Om något ämne (till exempel vatten) saknas från uttrycket för jämviktskonstanten eller från den beräkningsmässiga behandlingen av jämvikten (till exempel från tabellen eller insättningen) kan högst 2 p. ansamlas från deluppgiften (poängen för koncentrationerna i början).
- Om uppgiften har lösts med substansmängder i stället för koncentrationer ska man motivera att volymerna förkortas bort i jämviktskonstantens uttryck, annars avdras −2 p. för deluppgiften.
2,90 = x² / [(4,9767 – x) · (9,9661 – x)]
x = 4,0319 (eller x = 18,7753)
(1 p.)
Koncentrationerna ska vara positiva, så vi väljer x = 4,0319.
Jämviktskoncentrationerna: (2 p.)
c(nopol) = 4,9767 mol/l – 4,0320 mol/l = 0,9447 mol/l \approx 0,945 mol/l
c(ättiksyra) = 9,9661 mol/l – 4,0320 mol/l = 5,9341 mol/l \approx 5,93 mol/l
c(nopylacetat) = c(vatten) = 4,0320 mol/l \approx 4,03 mol/l
Poängsättning: två koncentrationer rätt, 1 p., de övriga två koncentrationerna rätt 1 p. (sammanlagt 2 p.)
Svar:
c(nopol) = 0,945 mol/l
c(ättiksyra) = 5,93 mol/l
c(nopylacetat) = c(vatten) = 4,03 mol/l
Del 3: 20-poängsuppgifter
9. Överhettning av en litiumjonackumulator 20 p.
Litiumjonackumulatorer används ofta i laddbar elektronik och i elbilar. Olika slags kemiska föreningar kan användas för att tillverka ackumulatorerna. Ofta använder man litiumkoboltoxid, LiCoO₂, som anodmaterial och grafit som katodmaterial. Som elektrolyt använder man vanligen något organiskt ämne och salter som gör det möjligt för litiumjonerna att röra sig. Totalreaktionen för uppladdning av ackumulatorn är
LiCoO₂(s) → Li(s) + CoO₂(s).
Litiumet som är i grundämnesform fäster sig vid ytan av grafitelektroden.
9.1 Varför kan man inte använda en vattenlösning som elektrolyt i en litiumjonackumulator? 3 p.
Litium i grundämnesform reagerar med vatten (2 p.) (och oxideras omedelbart).
Motivering eller precisering, 1 p., till exempel:
- Litium är en alkalimetall (och är därför reaktiv)
- Litium oxideras kraftigt
- Litium är ett kraftigt reduktionsmedel
- Litium reagerar kraftigt / häftigt
- Reaktionen är (mycket) exoterm / frigör (rikligt med) värme.
Ett alternativt sätt att svara:
Vattnet skulle reduceras istället för litium (vid uppladdningen). (2 p.)
Motivering med hjälp av normalpotentialerna (1 p.)
9.2 Då litiumkoboltoxid upphettas börjar den sönderfalla och det bildas litiumoxid i fast form, kobolt(II)oxid i fast form och syre. Skriv reaktionsformeln (reaktionslikheten) för sönderfallsreaktionen. Beräkna reaktionsentalpin för sönderfallsreaktionen för LiCoO₂ genom att använda bildningsentalpierna i tabell . 6 p.
Reaktionsformeln är:
4LiCoO₂(s) → 2Li₂O(s) + 4CoO(s) + O₂(g).
(3 p.)
Poängsättning: alla ämnen rätt, 1 p., koefficienterna rätt, 1 p., aggregationstillstånden rätt, 1 p. Poängen för koefficienterna och aggregationstillstånden kan ansamlas bara om ämnena är rätt.
- Koefficientfel eller felaktiga ämnen i reaktionen leder till att inga poäng kan ansamlas för entalpiberäkningen (ej-FF).
Reaktionsentalpin:
∆Hr(sönderfallsreaktionen)
= 2 · ∆Hf(Li₂O) + 4 · ∆Hf(CoO) + ∆Hf(O₂) – 4 · ∆Hf(LiCoO₂)
(1 p.)
= 2 · (–595,8 kJ/mol) + 4 · (–237,7 kJ/mol) + (0 kJ/mol) – 4 · (–679,4 kJ/mol)
(1 p.)
= 575,2 kJ/mol.
(1 p.)
- Som enhet godkänns kJ/mol eller kJ (också J/mol eller J).
- Om enheten saknas eller är fel, −1 p.
9.3
Syret som frigjorts i sönderfallsreaktionen för LiCoO₂ kan reagera vidare med de organiska ämnena i elektrolyten. Ett exempel på ett sådant ämne är etylenkarbonat C₃H₄O₃. Förbränningsreaktionen för det här ämnet är
2C₃H₄O₃(s/l) + 5O₂(g) → 6CO₂(g) + 4H₂O(g). ∆Hr = –4 510 kJ/mol
Utnyttja förbränningsreaktionen för etylenkarbonat samt sönderfallsreaktionen för LiCoO₂ som du skrev i deluppgift 9.2 och skriv reaktionsformeln för totalreaktionen mellan LiCoO₂ och etylenkarbonat. Vi antar att temperaturen är så hög att litiumkoboltoxiden sönderfaller på det sätt som beskrevs i deluppgift 9.2. Du kan använda molekylformler i reaktionsformeln.
Beräkna därtill reaktionsentalpin för totalreaktionen.
6 p.Totalreaktionen:
10LiCoO₂(s) + C₃H₄O₃(s/l) → 5Li₂O(s) + 10CoO(s) + 3CO₂(g) + 2H₂O(g)
(3 p.)
Poängsättning för totalreaktionen: alla ämnen rätt, 1 p., om därtill alla koefficienter är rätt, 2 p.
- Koefficientfel eller felaktiga ämnen i reaktionen leder till att inga poäng kan ansamlas för entalpiberäkningen (ej-FF).
Reaktionsentalpin för totalreaktionen
∆Hr(totalreaktionen) = (5 · ∆Hr(sönderfallsreaktionen) + ∆Hr(förbränningsreaktionen))/2
= (5 · (575,2 kJ/mol) + (–4 510 kJ/mol))/2
(1 p.)
= –817 kJ/mol.
(2 p.)
- Som enhet godkänns kJ/mol eller kJ (också J/mol eller J).
- Om enheten saknas eller är fel, −1 p.
9.4 Ifall en litiumjonackumulator får något fel kan den upphettas för mycket. Ett sådant fel kan uppstå till exempel vid en störning i funktionen för strömkretsen som övervakar ackumulatorns laddningsnivå. Diskutera varför en överhettning av litiumjonackumulatorn kan leda till en mycket farlig situation. 5 p.
Då litiumkoboltoxiden upphettas börjar syre frigöras. (2 p.)
- Om det därtill beskrivits i svaret att det frigjorda syret kan reagera med elektrolyten kan 1 p. till ansamlas.
Övriga observationer som sammanlagt ansamlar högst 3 p.:
- Som en följd av gasutvecklingen eller den exotermiska reaktionen går ackumulatorhöljet sönder / exploderar ackumulatorn. (1 p.)
- Om det därtill beskrivs att luftens syre då reagerar med litiumet eller elektrolyten, (1 p.).
- Ackumulatorn antänds eller förorsakar en eldsvåda (det här förutsätter att eldsvådan har kopplats till ackumulatorn eller till reaktionen i ackumulatorn). (1 p.) (Enbart konstaterande att en eldsvåda uppstår räcker alltså inte till för poäng.)
- Det är svårt att släcka en ackumulatorbrand. (1 p.)
10. Det smärtstillande läkemedlets gåta 20 p.
Tramadol är ett syntetiskt smärtstillande läkemedel som kom ut på marknaden på 1970-talet. Senare har man även funnit tramadol i Kamerun i Afrika, i rötter av träd som hör till släkten Nauclea. Det kan vara första gången som ett läkemedel som producerats av människan även återfunnits i naturen. Senare har man dock framlagt bevis på att tramadolen trots allt skulle ha hamnat i trädrötterna via avföring och urin från boskap och att den alltså inte skulle vara ett naturämne.
Du kan utnyttja material då du gör deluppgifterna.
10.1 Tramadol reagerar med syror så att reaktionsprodukten är ett salt. Vilken funktionell grupp i tramadol reagerar då? Rita strukturformeln för saltet som bildas av (+)-tramadol (K) och väteklorid (HCl). 4 p.
Aminogruppen reagerar. (1 p.)
- Godkänns ej: amingruppen / aminen
Strukturformeln för saltet (3 p.)
- Små fel, −1 p., till exempel
- en enskild väteatom saknas från andra ställen än funktionella grupper
- OH eller NH har bundits fel väg (bindningen till väteatomen).
- Betydande fel, −2 p., till exempel
- saltets +-laddning har ritats ut vid fel atom
- en metylgrupp saknas vid den protonerade aminogruppen.
- 0 p. för strukturen till exempel om:
- kloridjonen saknas
- en kovalent bindning har ritats ut mellan aminogruppen och kloridjonen
- valensfel (till exempel fem bindningar till en kolatom).
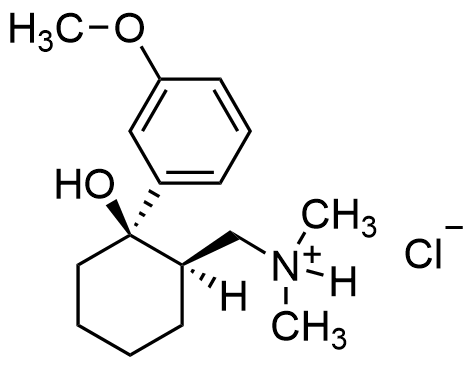 Strukturen för saltet som bildas
Strukturen för saltet som bildas
10.2 (+)-Tramadol (K) kan reagera i en elimineringsreaktion och då bildas två olika isomerer. Rita strukturformlerna för de här isomererna. 6 p.
3 p./isomer
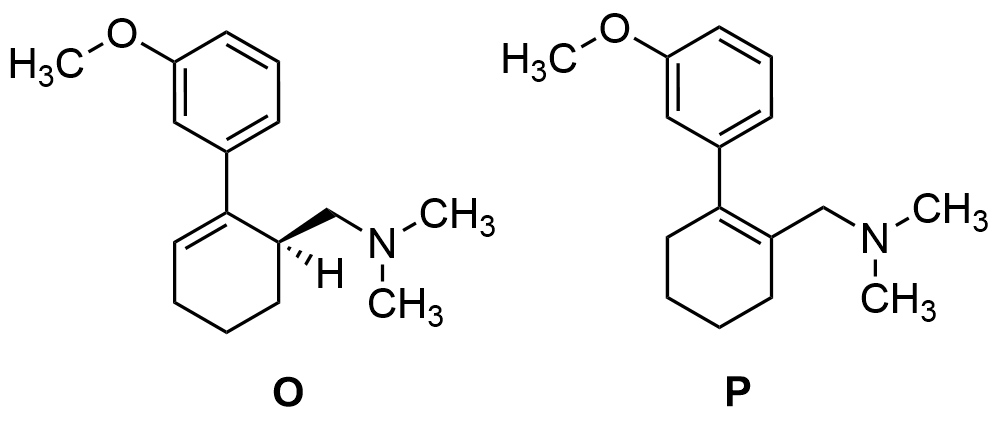 De rätta isomererna]
De rätta isomererna]
I struktur O krävs inte en beskrivning av stereokemin.
- Om dubbelbindningen är utritad på fel ställe eller fel grupp har eliminerats, 0 p. för strukturen.
- Om svaret förutom en rätt struktur innehåller en felaktig struktur görs inget poängavdrag. Om två eller fler felaktiga strukturer ritats ut, 0 p. för deluppgiften.
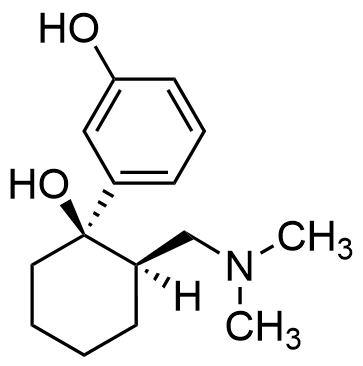
10.3 Etergruppen i (+)-tramadol (K) hydrolyseras i kroppen och då bildas en förening som innehåller en fenolgrupp. Den här föreningen är upp till hundra gånger mer effektiv som smärtstillande läkemedel jämfört med det ursprungliga läkemedlet. Rita strukturformeln för den här sönderfallsprodukten. 4 p.
10.4
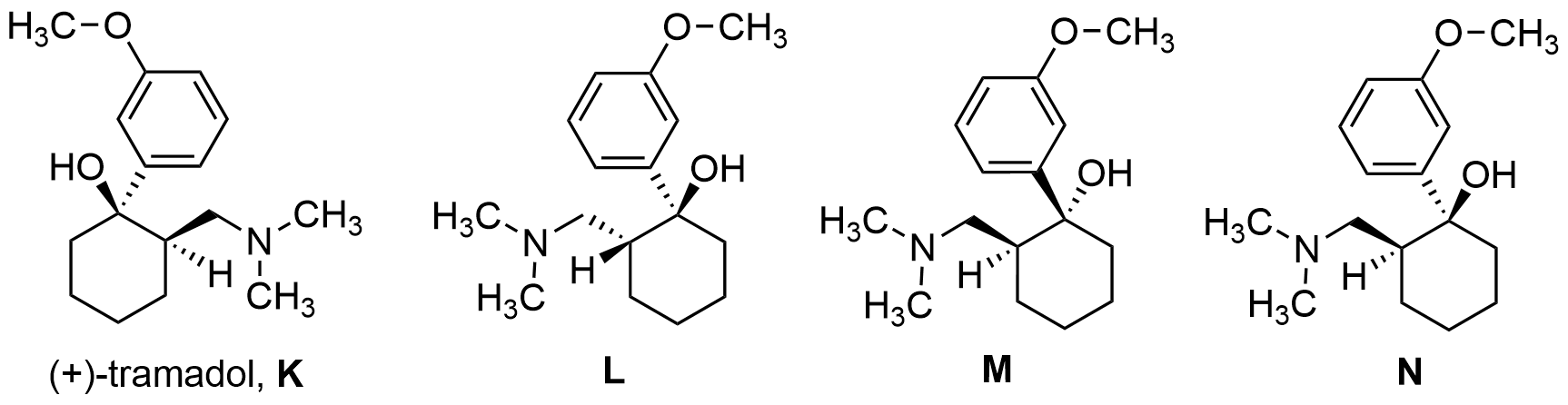
I syntesen av tramadol bildas en blandning av isomererna K ((+)-tramadol), L, M och N . Två av isomererna separeras ur blandningen och då blir läkemedlets verksamma ämne kvar som ett racemat (en racemisk blandning) bestående av (+)- och (−)-tramadol. Förklara vad racemat (racemisk blandning) betyder.
Vilken av isomererna L, M eller N är (−)-tramadol? Ifall tramadol bildades i naturen, skulle det då vara sannolikt att den skulle förekomma som ett racemat?
6 p.
En racemisk blandning innehåller lika mycket (1:1, 50:50) av båda enantiomererna, alltså i det här fallet av (+)- och (−)-tramadol. (2 p.)
Poängsättning: innehåller av båda enantiomererna, 1 p., i lika stor mängd, 1 p.
- Fel form av isomeri eller formen av isomeri är inte preciserad, 0 p.
Förening N är en enantiomer till (+)-tramadol. N måste vara (−)-tramadol. (2 p.)
I naturen styr (kirala) enzymer / proteiner bildandet av föreningar
ELLER
Enzymer / proteiner katalyserar enbart bildandet av den ena enantiomeren. (1 p.)
- Poängen förutsätter att protein eller enzym nämns i svaret.
Slutsatsen: och därför bildas bara den ena enantiomeren. (1 p.)
- Slutsatsens poäng kan ansamlas bara om den föregående poängen har förtjänats.
11. Infrarödspektroskopi 20 p.
11.1
Du har ett prov som du vet består av en ren förening. Du vet också att den här föreningen är en av två möjliga föreningar. Hur kan man med hjälp av IR-spektroskopi klargöra vilkendera föreningen provet innehåller?
IR-spektroskopi räcker inte nödvändigtvis till för att entydigt bestämma molekylens struktur. Namnge någon analysmetod som ger dig vidare information för identifieringen. Det räcker att du skriver analysmetodens namn i svaret.
6 p.
Vi uppmäter spektrumet för den okända föreningen.
Klargörande av föreningen, alternativ 1, högst 4 p.
Vi bestämmer vågtalen (1 p.) för absorptionstopparna i spektrumet. (1 p.)
Vi använder en tabell för att identifiera de funktionella grupper som spektrumets toppar motsvarar. (1 p.)
Vi jämför de funktionella grupperna som finns i strukturerna för de två möjliga föreningarna med den information spektrumets toppar ger oss och försöker identifiera provet. (1 p.)
Klargörande av föreningen, alternativ 2, högst 4 p.
Vi jämför spektrumet som vi uppmätte för föreningen med ett referensämnes spektrum. (2 p.)
Vi identifierar föreningen utifrån hur väl spektrumen stämmer överens med varandra. Spektrumens absorptionstoppars (1 p.) vågtal (och form) ska motsvara varandra. (1 p.)
Namngivning av en annan analysmetod, 2 p.:
Om IR-spektroskopi inte räcker till för att identifiera föreningen kan vi använda till exempel någon av följande analysmetoder: masspektrometri, NMR, UV-Vis (eller någon annan lämplig analysmetod). (2 p.)
- Som analysmetod godkänns inte separationsmetoder eller andra metoder som inte ger tilläggsinformation för identifieringen, till exempel: extraktion, centrifugering, destillering, indunstning, filtrering.
11.2 Vilkendera bindningens vibrationer har större vågtal, C–O-bindningens eller C=O-bindningens? Motivera. Du kan utnyttja text i ditt svar. 4 p.
C=O-bindningen är starkare än C–O-enkelbindningen. (2 p.)
Då är kraftkonstanten för C=O-bindningen större. (1 p.)
Därför har C=O-bindningens vibrationer ett högre vågtal. (1 p.)
11.3 Man kan också undersöka vibrationerna för bindningar mellan molekyler med hjälp av spektroskopi. Är vågtalen för vibrationerna för bindningar mellan molekylerna mindre eller större än vågtalen för bindningar inom en molekyl? Motivera. Du kan utnyttja text i ditt svar. 4 p.
Bindningarna mellan molekylerna är svagare än bindningarna inom molekylerna (2 p.), och därför är kraftkonstanterna för bindningarna mellan molekyler mindre (1 p.).
Vibrationerna för bindningarna mellan molekylerna har ett lägre vågtal än vibrationerna för bindningarna inom molekylerna. (1 p.)
11.4
Vätet i väteklorid (HCl) kan ersättas med vätets tyngre isotop ²H, alltså deuterium. Deuterium betecknas också med bokstaven D i molekylformler. Absorptionen som syns i IR-spektrumet för gasformig HCl har sin mittpunkt vid vågtalet \nu=2\ 890\ \mathrm{cm}^{-1}. Vågtalet för den motsvarande vibrationen i DCl är \nu=2\ 090\ \mathrm{cm}^{-1}.
Utnyttja text och beräkna förhållandet mellan de experimentella vibrationella vågtalen för HCl och DCl \left( \frac{\nu_{\mathrm{HCl}}} {\nu_{\mathrm{DCl}}} \right). Beräkna också motsvarande förhållande med hjälp av uttrycket för det harmoniska vågtalet. Du kan anta att bindningens kraftkonstant inte påverkas då väte ersätts med deuterium.
6 p.
Förhållandet mellan de experimentella vågtalen
\frac{\nu_{\mathrm{HCl}}}{\nu_{\mathrm{DCl}}} = \frac{2890\ \mathrm{cm}^{-1}}{2090\ \mathrm{cm}^{-1}}\approx 1,38
(1 p.)
Atomernas massor uttryckta i någon vettig enhet
mH: 1,008 u / 1,008 Da / 1,008 g/mol
mD: 2,014 u / 2,014 Da / 2,014 g/mol
(Som deuteriums massa godkänns till exempel mH + m(neutron), men en ur kemisk synvinkel felaktig princip godkänns inte, som till exempel 2 · mH)
mCl: 34,969 u / 34,969 Da / 34,969 g/mol (massan för ³⁵Cl; i uträkningen godkänns även den genomsnittliga molmassan för klor, 35,45 u)
(2 p.)
Poängsättning: Två massor rätt, 1 p. den tredje massan rätt, 1 p. (sammanlagt 2 p.).
Förhållandet mellan vågtalen som beräknats med uttrycket för det harmoniska vågtalet:
\mu_{\mathrm{DCl}}=\frac{m_\mathrm{D}m_\mathrm{Cl}}{m_\mathrm{D}+m_\mathrm{Cl}}=\frac{2{,}014\ \mathrm{u}\cdot 34{,}969\ \mathrm{u}}{2{,}014\ \mathrm{u} + 34{,}969\ \mathrm{u}}=\frac{70{,}428\ \mathrm{u}}{36{,}983\ \mathrm{u}}
\mu_{\mathrm{HCl}}=\frac{m_{\mathrm{H}}m_{\mathrm{Cl}}}{m_{\mathrm{H}}+m_{\mathrm{Cl}}}=\frac{1{,}008\ \mathrm{u}\cdot34{,}969\ \mathrm{u}}{1{,}008\ \mathrm{u}+34{,}969\ \mathrm{u}}=\frac{35{,}249\ \mathrm{u}}{35{,}977\ \mathrm{u}}
(1 p.)
- Rätt storhetsekvationer räcker till för poäng.
\frac{\nu_{\mathrm{HCl}}}{\nu_{\mathrm{DCl}}}=\frac{\frac{1}{2\pi c}\sqrt{\frac{k_\mathrm{HCl}}{\mu_\mathrm{HCl}}}}{\frac{1}{2\pi c}\sqrt{\frac{k_\mathrm{DCl}}{\mu_\mathrm{DCl}}}}=\sqrt{\frac{\mu_\mathrm{DCl}}{\mu_\mathrm{HCl}}}
(1 p.)
\frac{\nu_{\mathrm{HCl}}}{\nu_{\mathrm{DCl}}}=\sqrt{\frac{\frac{70{,}428}{36{,}983}\mathrm{u}}{\frac{35{,}249}{35{,}977}\mathrm{u}}}=\sqrt{\frac{35{,}977\cdot 70{,}428}{35{,}249\cdot 36{,}983}}\approx 1{,}39
(1 p.)