Hyvän vastauksen piirteet: FI – Kemia
26.3.2025
Lopulliset hyvän vastauksen piirteet 13.5.2025
Lopullisista hyvän vastauksen piirteistä ilmenevät perusteet, joiden mukaan koesuorituksen lopullinen arvostelu on suoritettu. Tieto siitä, miten arvosteluperusteita on sovellettu kokelaan koesuoritukseen, muodostuu kokelaan koesuorituksestaan saamista pisteistä, lopullisista hyvän vastauksen piirteistä ja lautakunnan määräyksissä ja ohjeissa annetuista arvostelua koskevista määräyksistä. Lopulliset hyvän vastauksen piirteet eivät välttämättä sisällä ja kuvaa tehtävien kaikkia hyväksyttyjä vastausvaihtoehtoja tai hyväksytyn vastauksen kaikkia hyväksyttyjä yksityiskohtia. Koesuorituksessa mahdollisesti olevat arvostelumerkinnät katsotaan muistiinpanoluonteisiksi, eivätkä ne tai niiden puuttuminen näin ollen suoraan kerro arvosteluperusteiden soveltamisesta koesuoritukseen.
Ylioppilastutkinnon kokeessa selvitetään, ovatko opiskelijat omaksuneet lukion opetussuunnitelman mukaiset tiedot ja taidot sekä saavuttaneet lukiokoulutuksen tavoitteiden mukaisen riittävän kypsyyden. Kemian kokeessa arvioinnin kohteina ovat kemiallisen tiedon ymmärtäminen ja soveltaminen. Arvioinnissa otetaan huomioon myös kokeellisen tiedonhankinnan ja ‐käsittelyn taidot. Näihin kuuluvat esimerkiksi kokeiden suunnittelu, työvälineiden ja reagenssien turvallinen käyttö, tulosten esittäminen ja tulkitseminen sekä johtopäätösten tekeminen ja soveltaminen.
Kemian tehtäviä arvosteltaessa painotetaan oppiaineen luonteen mukaista esitystapaa sekä käsitteiden ja kielenkäytön täsmällisyyttä. Reaktioyhtälöt esitetään ilman hapetuslukuja pienimmin mahdollisin kokonaislukukertoimin ja olomuodoilla varustettuna. Orgaanisissa reaktioyhtälöissä käytetään rakennekaavoja, mutta olomuotoja ei tarvitse mainita. Rakennekaavojen eri esitystavat hyväksytään.
Laskennallisissa tehtävissä suureyhtälöjä ja kaavoja käytetään tavalla, joka osoittaa kokelaan ymmärtäneen tehtävänannon oikein ja soveltaneen ratkaisussaan asianmukaista periaatetta tai lakia. Vastauksesta ilmenee yksiselitteisesti, miten lopputulokseen päädytään, mutta laajoja välivaiheita ei tarvita. CAS-ohjelmia voi hyödyntää tehtävän eri vaiheissa. Merkintätapojen kannalta keskeisiä vaiheita ovat periaatteiden ja lakien sekä lopputuloksen ja johtopäätösten esittäminen. Lopputulokset annetaan lähtöarvojen mukaisella tarkkuudella yksiköineen ja johtopäätökset perustellaan.
Mittaustuloksia ja niistä piirrettyjä kuvaajia hyödynnetään tiedon analysoinnissa ja johtopäätösten tekemisessä. Mittauspisteisiin sovitetaan asianmukainen suora. Mittauspisteiden välisiä arvoja voi interpoloida kuvaajaa silmämääräisesti lukemalla tai sopivalla ohjelmalla. Kuvaajaan merkitään akselien nimet, yksiköt ja asteikko. Kuvaajaan merkitään johtopäätösten kannalta olennaiset kohdat, kuten titrauskäyrän ekvivalenttikohta tai hetkellistä nopeutta laskettaessa kyseinen tangentti.
Essee‐ ja selittävissä vastauksissa tekstiä täydennetään reaktioyhtälöillä, kaavoilla tai piirroksilla. Käsiteltäviä ilmiöitä kuvataan makroskooppisella, mikroskooppisella ja symbolisella tasolla. Vastauksesta ilmenee, että tehtävään liittyvää aineistoa on hyödynnetty, sovellettu, analysoitu ja arvioitu tehtävänannon mukaisesti. Hyvä vastaus on jäsennelty ja sisällöltään johdonmukainen.
Vastaus arvostellaan tehtäväkohtaisten kriteerien mukaisesti. Lähtökohtana ovat vastauksen ansiot, joista kertyy pisteitä. Jos keskeinen kemiallinen periaate puuttuu tai se on virheellinen, pisteiden kertyminen päättyy. Tällöin virheellisen tuloksen siirtymistä eteenpäin ei hyväksytä (ei-VSE). Tällaiset virheet ovat esimerkiksi stoikiometriavirheet, väärä rajoittava tekijä tai väärä aine reaktioyhtälössä. Muiden puutteiden tai virheiden tapauksessa virheellisen tuloksen siirtyminen eteenpäin hyväksytään (VSE), jolloin pisteiden kertyminen jatkuu puutteen tai virheen jälkeen. Kokeen osan 3 vaativat tehtävät edellyttävät täsmällisempää periaatteiden hallintaa kuin kokeen alkupään perustehtävät. Kemian kannalta epätäsmällisestä kielenkäytöstä, pienestä laskuvirheestä tai likiarvojen huolimattomasta käytöstä vähennetään 0–3 p. esimerkiksi seuraavasti:
- pyöristys- ja kopiointivirheet, jotka eivät vaikuta lopputulokseen, −0 p.
- kopiontivirheet, pyöristysvirheet ja pienet huolimattomuusvirheet, jotka vaikuttavat lopputulokseen, yksittäinen pieni virhe rakennekaavassa −1 p.
- yksikönmuunnosvirheet, systemaattinen virhe rakennekaavassa tai muut vähäistä suuremmat virheet, jossa ei kuitenkaan ole väärä kemiallinen periaate −2 p.
Osa 1: 20 pisteen tehtävä
1. Monivalintatehtäviä kemian eri osa-alueilta 20 p.
1.1 Mikä seuraavista metalleista on neste tavanomaisissa laboratorio-olosuhteissa? 2 p.
- elohopea (2 p.)
1.2 Mikä seuraavista yhdisteistä on aldehydi? 2 p.
- propanaali (2 p.)
1.3 Mikä seuraavista liuoksista on emäksinen? 2 p.
- NaOH(aq) (2 p.)
1.4 Jos kaasupulloa lämmitetään, sen sisällä olevan kaasun 2 p.
- paine kasvaa. (2 p.)
1.5 Kaikki metallit 2 p.
- johtavat sähköä. (2 p.)
1.6 Polysakkarideissa monosakkaridit sitoutuvat toisiinsa 2 p.
- glykosidisidoksilla. (2 p.)
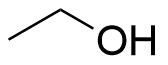
1.7 Mitkä olomuodon muutokset tapahtuvat, kun etanolia erotetaan vedestä tislaamalla? 2 p.
- Neste muuttuu kaasuksi ja uudelleen nesteeksi. (2 p.)
1.8 Mitä yhdistettä syntyy päätuotteena but-1-eenin ja vetybromidin välisessä additioreaktiossa? 2 p.
- 2-bromibutaania (2 p.)
1.9 Kemiallisessa reaktiossa energiaa vapautuu aina, kun 2 p.
- sidoksia muodostuu. (2 p.)
1.10 Erään reaktion lähtöaineen konsentraatiota kasvatetaan, jolloin reaktion nopeus kasvaa. Tämä johtuu siitä, että 2 p.
- molekyylien välisten törmäysten määrä kasvaa. (2 p.)
Osa 2: 15 pisteen tehtävät
2. Kaliumkloraatin hajoamisreaktio 15 p.
2.1
Kiinteä kaliumkloraatti KClO₃ voi hajota nopeassa eksotermisessä reaktiossa kiinteäksi kaliumkloridiksi KCl ja happikaasuksi O₂. Kirjoita tasapainotettu reaktioyhtälö.
Eräässä laboratoriokokeessa tutkittiin tätä hajoamisreaktiota käyttämällä lähtöaineena 2,34 grammaa kaliumkloraattia. Kuinka monta grammaa muodostui happikaasua?
10 p.
2KClO₃(s) → 2KCl(s) + 3O₂(g)
(3 p.)
-
Kaikki aineet oikein, 1 p.
-
Oikeiden aineiden lisäksi oikeat olomuodot, 1 p., ja oikeat kertoimet 1 p.
m(KClO₃) = 2,34 g
M(KClO₃) = 122,55 g/mol
(1 p.)
M(O₂) = 32,00 g/mol
(1 p.)
n(KClO₃) = m/M = (2,34 g) / (122,55 g/mol) = 0,019094 mol
(1 p.)
n(O₂) = 3/2 · n(KClO₃) = 3/2 · 0,019094 mol = 0,028641 mol
(2 p.)
-
Jos stoikometrinen suhde on väärä, pisteiden kertyminen päättyy
m(O₂) = n · M = 0,028641 mol · 32,00 g/mol = 0,91652 g ≈ 0,917 g
-
Hyväksytään vastauksena myös 0,92 g ja 0,9165 g. Muu numerotarkkuus, −1 p.
(2 p.)
2.2 Kaliumkloraattia voidaan käyttää yhtenä ainesosana tulitikun syttyvässä päässä. Mikä rooli kaliumkloraatilla on tulitikun syttymisessä? Perustele vastauksesi kemiallisesti. 2 p.
Tulitikku syttyy ja palamisreaktio voimistuu, koska kaliumkloraatin hajoaminen on lämpöä/energiaa vapauttava reaktio.
(1 p.)
-
Eksoterminen reaktio ei riitä pisteeseen. Eksotermisyys on mainittu tehtävänannossa.
Reaktiossa vapautuu lämpöä ja happikaasua. Happi tehostaa palamista.
(1 p.)
Kommentti: Todellisuudessa tulitikun syttymisprosessi on monimutkainen ja siihen liittyy useita aineita. Tämän tehtävän pisteitys perustuu tehtävänantoon ja lukiokemian mukaiseen tietoon.
2.3 Onko kaliumkloraatin hajoamisreaktio hapetus-pelkistysreaktio? Perustele vastauksesi. 3 p.
Kaliumkloraatin hajoamisreaktio on hapetus-pelkistysreaktio.
(1 p.)
-
Hapettumisreaktio / hapetusreaktio / pelkistymisreaktio / pelkistysreaktio, 0 p.
(Reagoivien aineiden hapetusluvut (hapetusasteet) muuttuvat.)
Kloorin hapetusluku muuttuu lähtöaineen luvusta +5 tuotteen lukuun −1
(1 p.)
ja hapen hapetusluku vastaavasti luvusta −2 lukuun 0.
(1 p.)
3. Epilepsialääkkeen valmistus 15 p.
3.1 Nimeä reaktioyhtälöstä ympyröidyt yhdisteiden O, P ja Q funktionaaliset ryhmät. 3 p.
O: aminoryhmä, P: esteriryhmä, Q: amidiryhmä
(3 p.)
-
Pisteitys: 1 p. / oikea ryhmä.
-
Ryhmän O nimenä ei hyväksytä amiinia.
3.2 Tunnista yhdisteet R ja S. Esitä kummankin yhdisteen nimi tai rakennekaava. 4 p.
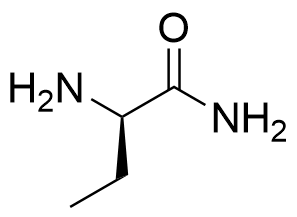
3.3 Tutkija haluaa valmistaa levetirasetaamin (Q) sijaan yhdisteen toista enantiomeeriä (peilikuvaisomeeriä). Tällöin tulee käyttää toista yhdistettä lähtöaineena yhdisteen O tilalla. Piirrä tämän toisen yhdisteen rakennekaava. 4 p.
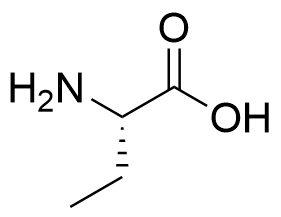
3.4 Yhdiste O voidaan valmistaa aminohaposta, jossa aminohapon karboksyyliryhmä muutetaan amidiryhmäksi. Piirrä tämän aminohapon rakennekaava. 4 p.
4. Lehtien väriaineet 15 p.
4.1 Selitä, miksi vaiheessa 1 lehtiä jauhetaan huhmareessa. Selitä, miksi näytettä sekoitetaan ja odotetaan 30 minuuttia. Nimeä käytetty erotusmenetelmä. 3 p.
Huhmareessa jauhaminen tekee lehtisilpusta hienojakoisempaa ja rikkoo kasvisoluja.
TAI
Huhmareessa jauhaminen edistää väriaineiden liukenemista uutossa.
(1 p.)
-
Pelkästään lehti muuttuu hienojakoisemmaksi, väriaineiden sekoittuminen veteen, tai lehden liukeneminen, 0 p.
Näytteen sekoittaminen keitinlasissa edistää väriaineiden liukenemista/uuttumista lehdistä vesiliuokseen.
TAI
Sekoittamisen jälkeen odotetaan 30 minuuttia, jotta liukenemista ehtisi tapahtua mahdollisimman paljon. (1 p.)
Ensimmäisen vaiheen nimi on (neste-kiinteä)uutto. (1 p.)
4.2 Kuvaile, mitä vaiheessa 2 tehdään. Nimeä käytetty erotusmenetelmä. 2 p.
Liuos suodatetaan büchnersuppilon läpi imupulloon, jolloin kiinteä lehtisilppu jää suppiloon ja väriaineita sisältävä vesiliuos päätyy imupulloon. (1 p.)
-
Jos liuoksen tilalla on vain vesi tai väriaineet , 0 p.
Toisen vaiheen erotusmenetelmä on (imu)suodatus. (1 p.)
4.3 Selitä, mitä videossa tapahtuu. Nimeä erotusmenetelmä ja kerro, mihin kemialliseen ominaisuuteen väriaineiden erottuminen perustuu. 5 p.
Kyseessä on (neste-neste)uutto. (1 p.)
Menetelmä perustuu siihen, että eroteltavat aineet liukenevat eri tavalla neste-nesteuutossa käytettyihin liuottimiin.
(1 p)
Korkeintaan 3 p. seuraavista tapahtumista ja niiden selityksistä. Piste edellyttää, että selitys on oikein:
-
Väriaineita sisältävä vesiliuos kaadetaan erotussuppiloon, johon lisätään dietyylieetteriä.
-
Selitys: Dietyylieetteri ei liukene veteen. / Dietyylieetteri liukenee vain vähän veteen(, joten muodostuu kaksi kerrosta). (1 p.)
-
-
Erotussuppiloa ravistetaan,
-
Selitys: Tämä lisää liuottimien välistä pinta-alaa. / Tämä nopeuttaa dietyylieetteriin paremmin liukenevien aineiden liukenemista dietyylieetterifaasiin. (1 p.)
-
-
Erotussuppilon hanaa avataan hetkeksi.
-
Selitys: Päästetään pois muodostunut kaasu. / Tasataan muodostunut paine. (1 p.)
-
-
Alempi faasi lasketaan erlenmeyerpulloon. Ylempi faasi kaadetaan yläkautta toiseen erlenmeyerpulloon.
-
Selitys: Tiheämpi faasi on alempana. / Faasi, jolla on pienempi tiheys on päällimmäisenä. (1 p.)
-
Selitys: Vesifaasi on alempana. / Vesifaasi on punaruskea. / Eetterifaasi on päällimmäisenä. / Eetterifaasi on keltainen. (1 p.)
-
4.4 Videon näyte sisältää kahta keltaista väriainetta: luteoliinia ja beetakaroteenia. Kuvassa on esitetty näiden molempien yhdisteiden rakennekaavat. Perustele yhdisteiden rakenteiden avulla, erottuvatko nämä yhdisteet videossa eri liuoksiin. 5 p.
Luteoliini on poolinen (1 p.). Se sisältää happiatomeja / pooliset OH-ryhmät / (fenolisia) hydroksiryhmiä / karbonyyliryhmä / eetteriryhmä (1 p.), jotka voivat muodostaa dipoli-dipolisidoksia tai vetysidoksia vesimolekyylien kanssa (1 p.). Luteoliini liukenee siis hyvin pooliseen veteen, mutta heikommin poolittomaan dietyylieetteriin.
Beetakaroteeni on pooliton. / Beetakaroteeni koostuu puolestaan vain hiilestä ja vedystä eikä sisällä poolisia ryhmiä (1 p.). Se liukenee siis paremmin poolittomaan dietyylieetterifaasiin (1 p.).
5. Tutkijan sekoilu 15 p.
5.1 Ensimmäiseksi tutkija päätti tehdä alkuaineanalyysin selvittääkseen yhdisteiden alkuainekoostumuksen massaprosentteina. Laite oli kuitenkin huollettavana, joten tutkija ei pystynyt tekemään analyysiä. Olisiko kunkin purkin sisällön yhdistäminen oikeaan rakenteeseen onnistunut alkuaineanalyysillä? Perustele vastauksesi. 4 p.
Yhdisteet L ja M ovat keskenään (rakenne)isomeerejä.
TAI
Yhdisteillä L ja M on sama molekyylikaava/suhdekaava.
(2 p.)
Tämän takia eri purkkien sisällön yhdistäminen oikeaan rakenteeseen ei onnistu alkuaineanalyysillä.
TAI
Yhdisteitä L ja M ei voida erottaa toisistaan alkuaineanalyysillä.
TAI
Yhdiste K eroaa massaprosenttiselta koostumukseltaan yhdisteistä L ja M, joten yhdiste K pystyttäisiin kuitenkin tunnistamaan.
(2 p.)
-
Jälkimmäiset 2 p. edellyttää, että edelliset 2 p. on saatu.
5.2 Tutkija liuotti pienen määrän jokaista yhdistettä veteen ja mittasi saatujen vesiliuosten pH-arvot. Purkin A sisältämän yhdisteen vesiliuos oli hieman hapan ja purkin B yhdisteen hieman emäksinen. Purkin C yhdiste ei muuttanut vesiliuoksen pH-arvoa. Mikä purkki sisälsi mitäkin yhdistettä? Perustele vastauksesi yhdisteiden rakenteiden perusteella. 6 p.
Pisteitys: Oikea kohdistus 1 p./yhdiste ja oikea perustelu 1 p./yhdiste.
Purkissa B oli yhdistettä K. / Purkin B sisältämän yhdisteen liuos oli emäksinen. (1 p.)
Yhdiste K sisältää aromaattisen aminoryhmän, ja siten se on heikko emäs. (1 p.)
Purkissa A oli yhdistettä L. Purkin A sisältämän yhdisteen liuos oli hapan. (1 p.)
Yhdiste L sisältää fenolisen hydroksiryhmän, ja siten se on heikko happo. (1 p.)
Purkissa C oli yhdistettä M. / Purkin C sisältämä yhdiste ei muuttanut vesiliuoksen pH-arvoa. (1 p.)
Yhdiste M ei sisällä funktionaalisia ryhmiä, jotka voivat toimia happona tai emäksenä vesiliuoksessa. (1 p.)
5.3
Tutkija mittasi vielä jokaisen yhdisteen ¹H-NMR-spektrin. Miksi yhdisteiden K, L ja M spektreissä oli eri määrät piikkejä?
Spektrissä 1 oli neljä piikkiä, spektrissä 2 oli viisi piikkiä ja spektrissä 3 oli kuusi piikkiä. Yhdistä spektrit 1, 2 ja 3 yhdisteisiin K, L ja M. Yhdistämistä ei tarvitse perustella.
5 p.
(¹H-NMR-spektroskopialla tutkitaan ¹H-ytimien virittymistä.) Erilaisissa kemiallisissa ympäristöissä olevista vety-ytimistä tulee kustakin piikki eri kohtaan spektriä (paikka ilmoitetaan tavallisesti kemiallisen siirtymän avulla). (Yhdisteessä K vetyjä on neljässä, yhdisteessä L viidessä ja yhdisteessä M kuudessa erilaisessa kemiallisessa ympäristössä.) Siksi yhdisteiden ¹H-NMR-spektrien piikkien määrät eroavat toisistaan. (2 p.)
-
Pisteisiin edellytetään, että on ymmärretty eri määrän spektripiikkejä johtuvan eri määrästä vety-ytimien kemiallisia ympäristöjä.
Spektri 1: yhdiste K
Spektri 2: yhdiste L
Spektri 3: yhdiste M
(3 p.)
-
1 p. / oikein kohdistettu yhdiste.
6. Voihappo 15 p.
6.1 Butaanihappo on heikko happo, jonka pKₐ-arvo on 4,82. Kuinka monta grammaa butaanihappoa pitää sekoittaa veteen, jotta muodostuneen liuoksen pH-arvo on 5,10, kun liuoksen lopputilavuus on 1,00 litraa? 10 p.
Liuoksen pH = 5,10 eli log₁₀[H₃O⁺] = −5,10.
[H₃O⁺] = 10−5,10 mol/l = 7,9433 ⋅ 10⁻⁶ mol/l
(1 p.)
Merkitään [H₃O⁺] = a ja ratkaistaan butaanihapon alkukonsentraatio, jota merkitään x. Merkitään butaanihappoa HA:lla.
Tasapainotarkastelu:
| HA | + | H₂O | ⇌ | A⁻ | + | H₃O⁺ | |
| Alussa (mol/l) | x | 0 | 0 | ||||
| Tasapainossa (mol/l) | x – a | a | a |
(2 p.)
-
Jos tasapainotarkastelu on väärin, osatehtävästä voi saada korkeintaan 4 p. (oksoniumionikonsentraation, Kₐ-arvon, Kₐ:n lausekkeen ja butaanihapon moolimassan pisteet)
pKₐ = 4,82 eli Kₐ = 10−4,82
(1 p.)
Kₐ = [H₃O⁺] [A⁻] / [HA]
(1 p.)
-
Jos Kₐ-arvon tilalla on käytetty pKₐ-arvoa, pisteiden kertyminen päättyy (ei-VSE).
= a² / (x–a)
(x-a) = a² / Kₐ
(1 p.)
x = a² / K + a = (10−5,10)² / 10−4,82 + 10−5,10 = 1,2112 ⋅ 10⁻⁵ (mol/l)
(1 p.)
m(HA) = n(HA) ⋅ M(HA) = (c(HA) · V) ⋅ M(HA)
M(HA) = 4 ⋅ 12,01 g/mol + 2 ⋅ 16,00 g/mol + 8 ⋅ 1,008 g/mol = 88,104 g /mol
(1 p.)
m(HA) = n(HA)·M(HA) = c(HA)·V·M(HA) = (1,2112 · 10⁻⁵ mol/l · 1,00 l) ⋅ 88,104 g /mol = 1,0671156 mg
Butaanihappoa pitää lisätä veteen 1,07 mg. (2 p.)
-
Yksikkönä hyväksytään sekä gramma että milligramma.
6.2 Ionit haihtuvat hyvin heikosti liuoksista. Tästä syystä butaanihapon haju johtuu lähinnä varauksettomien molekyylien konsentraatiosta liuoksessa. Opiskelija valmisti butaanihapon vesiliuoksen ja huomasi, että se haisee pahalta. Miten opiskelija voisi lieventää hajuhaittaa liuoksen pH:ta säätämällä? Perustele vastauksesi. 3 p.
Vastauksessa on tunnistettu, että haju johtuu varauksettomasta butaanihappomolekyylistä tai, että varauksettoman butaanihappomolekyylien määrää on pienennettävä.
(1 p.)
Koska butaanihappo on happo, varauksettoman molekyylin konsentraatio nesteessä pienenee, jos liuos muuttuu emäksisemmäksi. TAI
Opiskelija voi siis lievittää laboratorion hajuhaittaa kasvattamalla liuoksen pH:ta / neutraloimalla liuos.
(1 p.)
Emäs neutraloi hapon. / Emäs reagoi hapon kanssa. / Vastauksessa huomioitu butaanihapon happomuoto ja emäsmuoto.
(1 p.)
-
Vaihtoehtoisesti pisteet voi kerryttää tasapainoreaktiota tarkastelemalla:
-
Butaanihappo on heikko happo / butaanihapon protolyysi on tasapainoreaktio (1 p.).
-
pH-arvoa on nostettava (1 p.),
-
jolloin tasapaino siirtyy tuotteiden puolelle (1 p.).
-
6.3 Eräät butaanihaposta valmistetut yhdisteet tuoksuvat hyvältä, ja niitä käytetäänkin hajusteissa ja ruokatarvikkeissa. Esimerkiksi metyylibutanaatin tuoksu on hedelmäinen ja muistuttaa omenaa. Nimeä reaktiotyyppi, jonka avulla butaanihaposta voidaan tuottaa metyylibutanaattia. 2 p.
Esteröintireaktio (tai substituutioreaktio tai kondensaatioreaktio). (2 p.)
7. Galvaaninen kenno ja elektrolyysikenno 15 p.
7.1
Opiskelijan tehtävänä on rakentaa galvaaninen kenno. Hänellä on käytettävissään magnesiumkloridin vesiliuos, kupari(II)kloridin vesiliuos, kuparilevy, magnesiumlevy sekä muut tarvittavat välineet.
Täydennä virkkeet lisäämällä sopiva sana tai lukuarvo tyhjiin kohtiin.
7 p.
7.1.1 1 p.
magnesiumlevyä / magnesiumia (1 p.)
7.1.2 1 p.
kuparilevyä / kuparia (1 p.)
7.1.3 1 p.
magnesium (1 p.)
-
Ei hyväksytä: anodi, epäjalompi.
7.1.4 1 p.
kupari-ionit (1 p.)
-
Tässä tapauksessa hyväksytään myös kupari (tehtävänannon muotoilua huomioiden).
-
Ei hyväksytä: kuparilevy, kuparikloridi, katodi.
7.1.5 1 p.
2,71 V TAI 2,71 (1 p.)
7.1.6 1 p.
johtimella (1 p.)
-
hyväksytään erilaiset johtimen synonyymit
-
ei hyväksytä pelkästään laitetta, esimerkiksi polttimo, jännitemittari, virtapiiri
7.1.7 1 p.
7.2
Seuraavaksi tarkastellaan elektrolyysilaitteistoa, jossa elektrolysoidaan magnesiumkloridia ja kupari(II)kloridia sisältävää sulatetta. Oletetaan, että normaalipotentiaaliarvot ovat sulatteessa samat kuin vesiliuoksessa.
Perustele, mikä aine pelkistyy ja mikä hapettuu ensimmäisenä tässä elektrolyysissä.
3 p.
Hapettuva aine: kloridi-ioni hapettuu (kloorikaasuksi) (koska muut ionit ovat jo hapettuneessa muodossa). (1 p.)
Pelkistyvä aine: kupari-ioni pelkistyy ensin (1 p.).
Perustelu:
Kuparin pelkistymispotentiaali on korkeampi kuin magnesiumin.
TAI
Kloridi-ioni on ainut aine joka voi hapettua tässä elektrolyysissä.
(1 p.).
-
Vastauksessa tulee käydä ilmi, että kyse on kupari-ionista ja kloridi-ionista, joko sanallisesti tai kemiallisina symboleina.
-
Perustelupiste edellyttää, että sekä hapettuva että pelkistyvä aine ovat oikein.
7.3 Selitä kolme olennaista eroa, miten osatehtävän 7.2 elektrolyysikennon rakenne ja toiminta eroavat osatehtävän 7.1 galvaanisen kennon rakenteesta ja toiminnasta. 5 p.
Vastauksessa kuvataan galvaanisen kennon ja elektrolyysikennon rakenteelliset ja toiminnalliset eroavaisuudet (1–2 p. jokaisesta kuvatusta eroavaisuudesta, yhteensä enintään 5 p.).
-
Pisteitys:
-
Ensimmäinen rakenteellinen ero, 2 p.
-
Ensimmäinen toiminnallinen ero, 2 p.
-
Toinen rakenteellinen tai toiminnallinen ero 1 p. / kuvattu ero.
-
-
Vertailussa on kuvattava sekä galvaanista kennoa että elektrolyysikennoa ja kuvaukset eivät saa olla ristiriidassa tehtävänannon kanssa, eli vertailujen pitää sopia osatehtävien 7.1 ja 7.2 mukaisiin tilanteisiin. Esimerkiksi vesiliuoksen elektrolyysiä ei tässä hyväksytä.
Rakenteelliset erot, esimerkiksi:
-
Astia: Elektrolyysikennossa molemmat elektrodit ovat samassa astiassa. Galvaanisessa kennossa elektrodit ovat eri puolikennoilla.
TAI Galvaanisessa kennossa elektrolyytit yhdistetään suolasillalla, mutta elektrolyysikennossa ei käytetä suolasiltaa. -
Kennojen napaisuus: Elektrolyysikennossa anodi on positiivinen elektrodi ja katodi negatiivinen, mutta galvaanisessa kennossa anodi on negatiivinen elektrodi ja katodi positiivinen.
-
Sähköisen energian ja kemiallisen energian suhde: Elektrolyysikenno tarvitsee jännitelähteen. / Elektrolyysikenno kuluttaa sähköenergiaa. Galvaaninen kenno on jännitelähde. / Galvaaninen kenno tuottaa sähköenergiaa. / Galvaaniseen kennoon kytketään jännitemittari/kuorma.
-
Galvaanisessa kennossa elektrolyytit ovat suolojen vesiliuoksia. Elektrolyysikennossa elektrolyyttinä on suolasulate.
-
Galvaanisessa kennossa elektrodit ovat eri materiaalia. Elektrolyysikennossa elektrodit voivat olla samaa materiaalia.
Toiminnalliset erot, esimerkiksi:
-
Hapettumis-pelkistymisreaktion spontaanius: Reaktio on pakotettu elektrolyysikennossa, mutta spontaani galvaanisessa kennossa.
-
Elektrodit: Elektrolyysikennossa käytetään useimmiten passiivisia/inerttejä elektrodeja, kuten grafiittia tai platinaa. Galvaanisen kennon elektrodit voivat olla reaktioon osallistuvia tai passiivisia. / Galvaanisen kennon elektrodit ovat eri metalleja.
-
Galvaaninen kenno tuottaa sähköenergiaa. Elektrolyysikenno kuluttaa sähköenergiaa.
-
Hapettuminen ja pelkistyminen: Elektrolyysissä kloridi-ionit hapettuvat kloorikaasuksi, kun taas kupari- ja/tai magnesiumionit pelkistyvät alkuainemuotoon/kupariksi/magnesiumiksi. Galvaanisessa kennossa magnesium / epäjalompi metalli hapettuu kationeiksi ja kupari-ionit / jalomman metallin ionit pelkistyvät alkuainemuotoon/kupariksi.
TAI
Elektrolyysissä anionit / negatiiviset ionit hapettuvat alkuainemuotoon ja kationit pelkistyvät alkuainemuotoonsa. Galvaanisessa kennossa usein alkuainemuodossa oleva anodi hapettuu kationeiksi, kun taas jalomman aineen kationit pelkistyvät alkuainemuotoon.
8. Tasapainovakion määrittäminen 15 p.
Tutkija halusi selvittää rauta(III)-ionin ja tiosyanaatti-ionin välisen reaktion tasapainovakion arvon tietyssä lämpötilassa. Reaktiossa syntyy punainen koordinaatiokompleksi-ioni [Fe(SCN)]²⁺ seuraavan reaktioyhtälön mukaisesti:
Fe³⁺(aq) + SCN⁻(aq) ⇌ [Fe(SCN)]²⁺(aq)
8.1 Tutkija määritti spektrofotometrisesti liuoksen [Fe(SCN)]²⁺-ionikonsentraation. Kuvassa on esitetty [Fe(SCN)]²⁺-liuoksen absorptiospektri näkyvän valon aallonpituudella. Millä aallonpituudella absorbanssi pitää lukea [Fe(SCN)]²⁺-ionikonsentraation määrittämiseksi? Perustele vastauksesi. 3 p.
Absorbanssi kannattaa lukea sen maksimikohdasta (1 p.), joka on noin aallonpituudella 460 nm (1 p.). Kun absorbanssi luetaan maksimikohdasta, saadaan eri mittausten väliset erot mahdollisimman suuriksi; näin määrityksen herkkyys (tarkkuus) paranee ja voidaan analysoida pienempiä pitoisuuksia. (1 p.)
-
Hyväksytään aallonpituuden arvoja 450 nm–470 nm.
8.2
Tutkija valmisti standardiliuokset ja mittasi niiden absorbanssit valitulla aallonpituudella. Standardiliuosten pitoisuudet ja absorbanssit on esitetty taulukossa .
Sen jälkeen tutkija valmisti reaktioliuoksen sekoittamalla rauta(III)-ionia ja tiosyanaatti-ionia sisältävät liuokset. Reaktioliuoksen absorbanssi valitulla aallonpituudella on 0,757.
Piirrä standardisuoran kuvaaja ja laske reaktioliuoksen [Fe(SCN)]²⁺-ionin konsentraatio.
6 p.
A = 4704,1 l/mol ⋅ c − 0,0005676
(4 p.)
Kuvaajan ja yhtälön pisteitys:
-
Akselit oikein päin, 1 p.
-
Akselien nimet ja yksiköt oikein, 1 p.
-
Kuvaajalla oikeat mittapisteet ja sovitettu oikea suora, 1 p.
-
Jos sovitus ei ole lineaarinen tai sovitusta ei ole lainkaan tehty, osatehtävästä saa korkeintaan 2 p. (jos akselit ovat oikein päin ja nimetty oikein)
-
Pisteen (0,0) pois jättämisestä vähennetään 1 p.
-
-
Yhtälö oikein, 1 p.
Yhtälön avulla ratkaistaan tuntemattoman näytteen konsentraatio:
c = (0,757 + 0,0005676) / (4704,1 l/mol) = 1,6105 ⋅ 10⁻⁴ mol/l = 1,61 ⋅ 10⁻⁴ mol/l
(2 p.)
-
Jos konsentraatio on määritetty kuvaajasta laskinohjelman avulla edellytetään, että piste on luettu absorbanssin arvolla, joka pyöristyy arvoon 0,757.
8.3
Tutkija valmisti uuden reaktioliuoksen lisäämällä 10 ml:n mittapulloon 2,00 ml Fe(NO₃)₃-liuosta, jonka konsentraatio oli 5,00 ⋅ 10⁻³ mol/l, sekä 3,00 ml KSCN-liuosta, jonka konsentraatio oli 3,00 ⋅ 10⁻³ mol/l, ja täyttämällä mittapullon vedellä merkkiin saakka. Syntyneen liuoksen [Fe(SCN)]²⁺-ionin tasapainokonsentraatio oli absorbanssin perusteella 8,12 ⋅ 10⁻⁵ mol/l.
Laske muiden reaktioon osallistuvien ionien tasapainokonsentraatiot sekä reaktion tasapainovakion arvo.
6 p.
Lasketaan ionien konsentraatiot alussa:
n(Fe³⁺) = 5,00 ⋅ 10⁻³ mol/l ⋅ 2,00 ⋅ 10⁻³ l = 1,00 ⋅10⁻⁵ mol
n(SCN⁻) = 3,00 ⋅ 10⁻³ mol/l ⋅ 3,00 ⋅ 10⁻³ l = 9,00 ⋅10⁻⁶ mol
(1 p.)
c(Fe³⁺) = 1,00 ⋅ 10⁻⁵ mol / (10,00 ⋅ 10⁻³ l) = 1,00 ⋅10⁻³ mol/l
c(SCN⁻) = 9,00 · 10⁻⁶ mol / (10,00 · 10⁻³ l) = 9,00 · 10⁻⁴ mol/l
(1 p.)
-
Tehtävä perustuu ionien konsentraatioihin. Jos vastauksessa käsitellään ainoastaan suolojen konsentraatiot, 0 p. osatehtävästä. Kalium- ja nitraatti-ionit eivät osallistu tasapainoreaktioon.
Tasapainotilanteen tarkastelu:
| Fe³⁺(aq) | + | SCN⁻(aq) | ⇌ | [Fe(SCN)]²⁺(aq) | |
|
Alussa (mol/l) | 1,00 ⋅10⁻³ | 9,00 ⋅10⁻⁴ mol | 0 | ||
|
Muutos (mol/l) | −x | −x | +x | ||
| Tasapainossa | 1,00 ⋅10⁻³ mol/l− x | 9,00 ⋅10⁻⁴ mol/l − x | x = 8,12 ⋅ 10⁻⁵ mol/l |
Tasapainokonsentraatiot:
c(Fe³⁺) = 1,00 ⋅10⁻³ mol/l−x = 1,00⋅10⁻³ mol/l −8,12⋅10⁻⁵ mol/l = 9,188 ⋅ 10⁻⁴ mol/l
c(SCN⁻) = 9,00 · 10⁻⁴ mol/l – x = 9,00 · 10⁻⁴ mol/l – 8,12 · 10⁻⁵ mol/l = 8,188 · 10⁻⁴ mol/l
(2 p.)
-
Jos tasapainotarkastelussa on virheitä, voi osatehtävästä saada korkeintaan 3 p. (konsentraatiot alussa ja Kc:n lauseke).
-
Tasapainotarkastelua ainemäärillä ei hyväksytä.
Tasapainovakion laskeminen:
K_c =\frac{c\left(\left[\mathrm{Fe(SCN)}\right]^{2+}\right)}{c\left(\mathrm{Fe}^{3+} \right) \cdot c\left(\mathrm{SCN}^- \right)}
(1 p.)
Kc = 8,12 ⋅ 10⁻⁵ / (9,188 ⋅ 10⁻⁴ ⋅ 8,188 ⋅ 10⁻⁴) = 107,93 ≈108
Vastaus hyväksytään yksiköillä (108 l/mol) tai ilman yksikköä.
(1 p.)
Osa 3: 20 pisteen tehtävät
9. Ferraatti-ioni 20 p.
9.1
Mikä on raudan hapetusluku ferraatti-ionissa?
Myös kromi voi muodostaa hapen kanssa ioneja, joissa kromilla on sama hapetusluku kuin ferraatti-ionin raudalla. Kirjoita yhden tällaisen kromia ja happea sisältävän ionin kaava ja anna sen nimi.
4 p.
Raudan hapetusluku on +6 TAI +VI.
(2 p.)
-
Jos raudan hapetusluku on väärin, 0 p. osatehtävästä.
Kromaatti-ioni \mathrm{CrO}_4^{2-}
tai
Dikromaatti-ioni \mathrm{Cr_2O}_7^{2-}
(2 p.)
-
Oikea kaava, 1 p.
-
Oikea kaava nimetty oikein, 1 p.
9.2 Rautahappo on kahdenarvoinen happo. Kun rautahappo reagoi natriumhydroksidin kanssa, muodostuu natriumferraattia ja vettä. Kirjoita rautahapon molekyylikaava. 2 p.
H₂FeO₄
(2 p.)
-
Jos vety on kaavan keskellä, tai raudan ja hapen järjestys on päinvästainen, korkeintaan 1 p.
-
Vastauksena tulee antaa molekyylikaava.
9.3 Happamassa vesiliuoksessa ferraatti-ioni pelkistyy Fe³⁺-ioniksi. Reaktiossa syntyy myös vettä. Kirjoita puolireaktio, joka kuvaa ferraatti-ionin pelkistymistä happamissa olosuhteissa. Olomuotoja ei tarvitse merkitä näkyviin. 3 p.
\mathrm{FeO_4^{2-} + 8H^{+} + 3e^{-}} \rightarrow \mathrm{Fe^{3+}+4H_2O}
(3 p.)
-
Pisteitys:
-
Kaikki lähtöaineet, tuotteet ja elektronit oikein, 2 p.
-
Lisäksi kaikki kertoimet oikein, 1 p.
-
9.4 Natriumferraatin vesiliuosta voi valmistaa kuumentamalla kiinteää rauta(III)hydroksidia natriumhypokloriitin (NaClO) ja natriumhydroksidin vesiliuoksessa. Reaktiossa hypokloriitti-ioni toimii hapettimena pelkistyen itse kloridi-ioniksi. Kirjoita natriumferraatin valmistuksen reaktioyhtälö. 7 p.
2Fe(OH)₃(s) + 3NaClO(aq) + 4NaOH(aq) → 2Na₂FeO₄(aq) + 5H₂O(l) + 3NaCl(aq)
(7 p.)
Pisteitys:
-
Kaikki lähtöaineet oikein, 1 p.
-
Lisäksi kaikki tuotteet oikein, 3 p.
-
Oikeiden aineiden lisäksi kaikki kertoimet oikein 2 p., ja kaikki olomuodot oikein 1 p.
-
Reaktion voi kirjoittaa ionimuodossa edellyttäen, että se on tasapainotettavissa oikein, myös varauksien osalta. Esimerkiksi, jos muuten aineet on kirjoitettu neutraaleina yhdisteinä, mutta tuotteissa on erikseen kloridi-ioni, osatehtävästä korkeintaan 1 p., jos lähtöaineet oikein.
9.5 Happamissa olosuhteissa ferraatti-ionin pelkistymispotentiaali on +2,20 V, ja emäksisissä olosuhteissa se on +0,72 V. Perustele, miksi ferraatti-ionin vesiliuoksen pH-arvo kannattaa säätää emäksiseksi ennen sen varastointia. 4 p.
Veden hapettumispuolireaktion potentiaali on −1,23 V
TAI
2H₂O(l) → O₂(g) + 4H⁺ (aq) + 4e⁻ , E = −1,23 V.
(1 p.)
Happamissa olosuhteissa ferraatti-ionin pelkistymispotentiaalin ja veden hapettumispotentiaalin summa on positiivinen.
TAI
E = +2,20 V + (−1,23 V) = 0,97 V > 0 V
(1 p)
Emäksisissä olosuhteissa taas ferraatti-ionin pelkistymispotentiaalin ja veden hapettumispotentiaalin summa on negatiivinen.
TAI
E = +0,72 V + (−1,23 V) = −0,51 V < 0 V
(1 p)
-
Jos potentiaalin yksikkö (V) puuttuu kokonaan, −1 p.
Johtopäätös:
Happamissa olosuhteissa ferraatti-ioni alkaa hapettaa vettä ja pelkistyy itse Fe³⁺-ioniksi.
TAI
Happamissa olosuhteissa vesi pelkistää ferraatti-ionin Fe³⁺-ioniksi.
TAI
Emäksisissä olosuhteissa ferraatti-onin pelkistyminen ei tapahdu spontaanisti.
(1 p.)
-
Johtopäätöspiste voidaan ansaita vain, jos vähintään yksi edeltävistä pisteistä on ansaittu.
Vaihtoehtoinen, puutteellinen vastaus, jossa ei ole hyödynnetty puolireaktioiden normaalipotentiaaliarvoja, osatehtävästä korkeintaan 1 p., esimerkiksi:
Happamissa olosuhteissa ferraatti-ionin pelkistymispotentiaali on suurempi kuin emäksisissä olosuhteissa, joten ferraatti-ioni pelkistyy happamissa olosuhteissa helpommin.
10. Hiilimonoksidin poisto 20 p.
10.1 Anna esimerkki tilanteesta tai prosessista, jossa syntyy hiilimonoksidia. Kerro, millaisiin reaktio-olosuhteisiin hiilimonoksidin synty liittyy. 2 p.
Hiilimonoksidia syntyy epätäydellisen palamisen yhteydessä.
(1 p.)
-
Ei hyväksytä, että happi on rajoittavana tekijänä tai, että palaminen tapahtuu hapettomissa oloissa.
Hiilimonoksidia syntyy esimerkiksi polttomoottoriautoissa, teollisuuden polttoprosesseissa, taitamattoman puunpolton yhteydessä, tulipaloissa ja tupakoidessa.
(1 p.)
-
Yksi esimerkki riittää.
10.2 Miksi hiilimonoksidin kertyminen sisäilmaan on vaarallista? 3 p.
1 p. per huomio:
-
Hiilimonoksidi on myrkyllinen kaasu.
-
Hiilimonoksidi sitoutuu hemoglobiiniin / vereen hapen sijasta, mikä aiheuttaa häkämyrkytyksen.
-
Hiilimonoksidi muodostaa ilman kanssa erittäin helposti syttyvän kaasuseoksen.
-
Ihminen ei aisti hiilimonoksidia.
-
Hiilimonoksidi syrjäyttää huoneilman jos hiilimonoksidipitoisuus on hyvin korkea. (Tämä on epätodennäköinen tilanne ja edellyttää hyvin korkeita hiilimonoksidimääriä.)
10.3 Mitä haittoja ja vaaraominaisuuksia hiilidioksidilla CO₂ on? 2 p.
1 p. / haitallinen vaikutus tai vaaraominaisuus. Esimerkiksi:
-
Hiilidioksidi on suurina pitoisuuksina tukahduttavaa.
-
Lievästi kohonneina pitoisuuksina hiilidioksidi aiheuttaa esimerkiksi päänsärkyä ja väsymystä.
-
Hiilidioksidi on kasvihuonekaasu, joka aiheuttaa ilmaston lämpenemistä.
-
Hiilidioksidi happamoittaa vesistöjä.
Ei hyväksytä liian epätarkkoja vastauksia, esimerkiksi:
-
Hiilidioksidi on haitallinen terveydelle / ilmakehälle / vesistöille.
-
Hiilidioksidi syrjäyttää hapen verenkierrossa.
Selvästi vääristä vastauksista voidaan vähentää 1 p., esimerkiksi:
-
Hiilidioksidi hajottaa otsonikerroksen.
-
Hiilidioksidi on helposti syttyvä / räjähdysherkkä.
10.4
Hiilimonoksidin hapettumisreaktiossa tutkittiin uutta katalyyttiä. Hiilimonoksidia ja happea suljettiin paineastiaan huoneenlämpötilassa. Paine astiassa oli 102 kPa. Katalyytin avulla hiilimonoksidi reagoi kokonaan hiilidioksidiksi korotetussa lämpötilassa:
2CO(g) + O₂(g) → 2CO₂(g)
Kun reaktioastia oli jäähtynyt takaisin huoneenlämpöiseksi, paine astiassa oli 85 kPa. Kuinka monta tilavuusprosenttia hiilidioksidia seoksessa oli reaktion jälkeen?
13 p.
Tehtävään on monta erilaista ratkaisutapaa. Alla on kuvattu yksi tapa. Kaikissa ratkaisutavoissa pisteet (13 p.) kertyvät seuraavasti:
-
Hiilimonoksidin, hapen ja hiilidioksidin ainemäärät alussa ja lopussa hahmoteltu oikein (esimerkiksi tasapainotaulukon avulla), 3 p.
-
Jos tämä tarkastelu on virheellinen, tehtävästä voi saada korkeintaan 5 itsenäistä pistettä.
-
-
Kaasuseoksen kokonaisainemäärä sekä alussa että lopussa, 2 p.
-
Itsenäiset pisteet, yhteensä 5 p., on merkitty ip:llä alla olevassa kuvauksessa. Jos tehtävässä on jokin periaatevirhe, nämä pisteet voi kuitenkin kerryttää.
-
Loppuosa laskusta ja oikea vastaus, yhteensä 3 p.
p(alku) = 102 kPa
p(loppu) = 85 kPa
nₖₒₖ = kaasujen kokonaisainemäärä ennen reaktiota
| 2CO(g) | + | O₂(g) | → | 2CO₂(g) | |
| Alku (n/mol) | x | nₖₒₖ − x | 0 | ||
| Loppu (n/mol) | 0 | ( n ₖₒₖ − x ) − x/2 | x |
(3 p.)
Taulukosta saadaan kokonaisainemäärät alussa (CO ja O₂) ja lopussa (O₂ ja CO₂):
n(alku) = nₖₒₖ
n(loppu) = (nₖₒₖ − x) − x/2 + x = nₖₒₖ − x/2
(2 p.)
Ratkaisusta ilmenee, että happea on reaktioastiassa ylimäärin.
(1 ip.)
Reaktiossa tilavuus ja lämpötila pysyvät vakiona.
(1 ip.)
Kaavan pV = nRT perusteella paine on suoraan verrannollinen ainemäärään.
(1 ip.)
-
Pelkkä kaava ei riitä tähän pisteeseen.
Supistetaan pois vakiona pysyvät T, V ja R:
p(alku) · V = n(alku) · RT
p(loppu) · V = n(loppu) · RT
Jaetaan yhtälöt puolittain.
Saadaan: p(alku) / p(loppu) = n(alku) / n(loppu)
(2 ip.)
102 kPa / 85 kPa = nₖₒₖ / (nₖₒₖ – x/2)
Saadaan:
x = 1/3 · nₖₒₖ
Kaasun tilavuus on suoraan verrannollinen ainemäärään. CO₂:n tilavuusprosentti reaktion jälkeen:
Til.-%(CO₂) = V(CO₂) / V(CO₂+O₂) = [n(CO₂)RT / p] / [n(CO₂+O₂)RT / p] = n(CO₂) / n(CO₂+O₂)
Til.-%(CO₂) = x / (nₖₒₖ − x/2)
Sijoitetaan kaavaan x = 1/3 · nₖₒₖ
Til.-%(CO₂) = (1/3 · nₖₒₖ) / (nₖₒₖ – 1/3 · nₖₒₖ / 2)
= 40 %
(3 p.)
11. Vetytalous 20 p.
11.1 Vetyä voidaan varastoida ja kuljettaa kaasuna korkeassa paineessa. Miksi vetykaasun vuotaminen olisi vaarallista? 2 p.
1 p. / kohta:
-
Vetykaasu on herkästi syttyvä.
-
Vety reagoi ilman/hapen kanssa.
-
Voi tapahtua räjähdys tai tulipalo (tämä piste edellyttää, että syttyvyys tai reaktio ilman/hapen kanssa on kuvattu).
-
Vedyn palaminen on eksoterminen reaktio. / Palossa vapautuu kuumia kaasuja.
-
Tukehtumisvaara, jos vetyä kertyy suuri määrä suljettuun tilaan.
-
Vetyä on vaikea tunnistaa, koska se on väritön/hajuton/mauton.
11.2 Toinen tapa varastoida ja kuljettaa vetyä on nesteenä normaalipaineessa. Selitä vedyn rakenteen avulla, miksi normaalissa ilmanpaineessa vety pysyy nesteenä vain hyvin matalassa lämpötilassa. 3 p.
Enintään 3 p. seuraavista:
Vetymolekyyli on pooliton (1 p.). Siksi vetymolekyylien välille muodostuu vain dispersiovoimia. (1 p.). Koska vetymolekyyli on pienikokoinen ovat dispersiovoimat erityisen heikkoja (1 p.).
Vain hyvin matalassa lämpötilassa molekyylien kineettinen energia ei riitä kumoamaan dispersiovoimia molekyylien välillä. (1 p.)
-
Jos vetymolekyylien välille on kohdistettu muu vuorovaikutus kuin dispersiovoimat tai, jos kuvataan molekyylien sisäisten sidosten katkeamista, 0 p. osatehtävästä.
11.3 Vety on mahdollinen tulevaisuuden liikennepolttoaine. Mitä etuja ja haasteita liittyy vedyn käyttöön autojen energialähteenä? Voit hyödyntää vastauksessasi tekstiä . 5 p.
Vastauksessa kuvataan sekä etuja että haasteita, jotka liittyvät vedyn käyttöön autojen polttoaineena. Yhteensä enintään 5 p.
Etuja, 1 p. / kohta, enintään 3 p. Esimerkiksi:
-
Vettä (joka on elektrolyysissä vedyn lähtöaine) on paljon saatavilla.
-
Vedyn tuotanto aiheuttaa vain vähän hiilidioksidipäästöjä, jos elektrolyysiin tarvittava sähkö tuotetaan ei-fossiilisilla energianlähteillä.
-
Vedyn käyttö polttoaineena / polttokennossa ei tuota hiilidioksidipäästöjä vaan tuotteena syntyy vain vettä.
-
Vedyn tankkaaminen on nopeampaa kuin sähköauton lataaminen. TAI Polttokennoautoissa vedyllä tuotetaan kennossa sähköä, joten auto on lähes äänetön, mikä vähentää liikenteen meluhaittoja verrattuna polttomoottoriautoihin.
-
Vety sisältää paljon energiaa per massayksikkö.
-
Polttokennon hyötysuhde on hyvä.
Haasteita, 1 p. / kohta, enintään 3 p. Esimerkiksi:
-
Vetyä ei esiinny luonnossa vapaana.
-
Vedyn valmistys vaatii katalyyttejä/kriittisiä alkuaineita jotka ovat harvinaisia tai kalliita. TAI Vedyn valmistus tuottaa hiilidioksidipäästöjä jos käytetään fossiilisia energianlähteitä.
-
Erilaisia haasteita, jotka liittyvät vedyn säilyttämisen tai kuljettamisen. Esimerkiksi: Vedyn siirtäminen kaasuna tehokkaasti edellyttää, että putkistossa on korkea paine, jotta järkevään tilavuuteen saadaan mahtumaan merkittävä määrä vetyä. TAI vedyn siirtäminen nesteenä vaatii hyvin matalaa lämpötilaa. TAI Vedyn varastoimiseen tarvitaan korkeita paineita tai hyvin matalia lämpötiloja, mikä kuluttaa paljon energiaa ja on teknisesti haastavaa. TAI Jakeluverkostoa ei vielä ole, joten se pitäisi rakentaa.
-
Vety sisältää vähän energiaa per tilavuusyksikkö.
11.4 Selitä, miten vetyä voidaan hyödyntää energiatuotannossa. Miten vedyn käyttö vähentäisi hiilidioksidipäästöjä? Hyödynnä vastauksessasi kemian tietojasi ja tekstiä . 6 p.
Vedyn käyttö energiatuotannossa, enintään 5 p.:
Kun sähköä tuotetaan enemmän kuin käytetään, voitaisiin ylimäärä hyödyntää energiana elektrolyysissä, jossa tuotetaan vetyä vedestä (1 p.). Vetyä voidaan tällä tavalla tuottaa uusiutuvalla energialla (1 p.). Vetyä voidaan käyttää energialähteenä suoraan polttamalla (1 p.) tai esimerkiksi polttokennoissa (1 p.). Vedystä voidaan myös tuottaa muita aineita, kuten hiilivetyjä ja metanolia, joita on mahdollista käyttää polttoaineena (1 p.).
Hiilidioksidipäästöjen vähentäminen, enintään 2 p.:
-
Vedyn käyttö vaikuttaa suoraan siihen, että hiilidioksidipäästöjä ei synny, esimerkiksi: Kun poltetaan vetyä, syntyy vain vettä eikä hiilidioksidipäästöjä muodostu (1 p.).
-
Vedyn käyttö vaikuttaa välillisesti siihen, että hiilidioksidipäästöjä ei synny, esimerkiksi: Vedyn avulla tuotetulla energialla voidaan korvata fossiilisilla polttoaineilla tuotettua energiaa (1 p.).
11.5 Tutustu tekstiin . Miksi on energiatehokkaampaa tuottaa hiilivetyjä Fischer–Tropsch-prosessissa käyttämällä lähtöaineena hiilimonoksidia hiilidioksidin sijaan? Kuinka suuri on reaktioentalpia hiilidioksidimoolia kohden, kun lähtöaineena käytetään hiilidioksidia? 4 p.
Hiilidioksidin muuntaminen hiilimonoksidiksi on endoterminen prosessi.
(1 p.)
Kokonaisprosessi vaatii enemmän energiaa, jos lähtöaineena on hiilidioksidi.
(1 p.)
Kokonaisreaktion reaktioentalpia olisi
+41 kJ/mol + (−152 kJ/mol) = −111 kJ/mol.
(2 p.)