Hyvän vastauksen piirteet: FI – Kemia
20.3.2026
Alustavat hyvän vastauksen piirteet 20.3.2026
Alustavat hyvän vastauksen piirteet on suuntaa antava kuvaus kokeen tehtäviin odotetuista vastauksista ja tarkoitettu ensisijaisesti tueksi alustavaa arvostelua varten. Alustavat hyvän vastauksen piirteet eivät välttämättä sisällä ja kuvaa tehtävien kaikkia hyväksyttyjä vastauksia. Alustavat hyvän vastauksen piirteet eivät ole osa Ylioppilastutkintolautakunnan yleisissä määräyksissä ja ohjeissa tarkoitettua tietoa siitä, miten arvosteluperusteita on sovellettu yksittäisen kokelaan koesuoritukseen. Alustavat hyvän vastauksen piirteet eivät sido Ylioppilastutkintolautakuntaa lopullisen arvostelun perusteiden laadinnassa.
Ylioppilastutkinnon kokeessa selvitetään, ovatko opiskelijat omaksuneet lukion opetussuunnitelman mukaiset tiedot ja taidot sekä saavuttaneet lukiokoulutuksen tavoitteiden mukaisen riittävän kypsyyden. Kemian kokeessa arvioinnin kohteina ovat kemiallisen tiedon ymmärtäminen ja soveltaminen. Arvioinnissa otetaan huomioon myös kokeellisen tiedonhankinnan ja ‐käsittelyn taidot. Näihin kuuluvat esimerkiksi kokeiden suunnittelu, työvälineiden ja reagenssien turvallinen käyttö, tulosten esittäminen ja tulkitseminen sekä johtopäätösten tekeminen ja soveltaminen.
Kemian tehtäviä arvosteltaessa painotetaan oppiaineen luonteen mukaista esitystapaa sekä käsitteiden ja kielenkäytön täsmällisyyttä. Reaktioyhtälöt esitetään ilman hapetuslukuja pienimmin mahdollisin kokonaislukukertoimin ja olomuodoilla varustettuna. Orgaanisissa reaktioyhtälöissä käytetään rakennekaavoja, mutta olomuotoja ei tarvitse mainita. Rakennekaavojen eri esitystavat hyväksytään.
Laskennallisissa tehtävissä suureyhtälöjä ja kaavoja käytetään tavalla, joka osoittaa kokelaan ymmärtäneen tehtävänannon oikein ja soveltaneen ratkaisussaan asianmukaista periaatetta tai lakia. Vastauksesta ilmenee yksiselitteisesti, miten lopputulokseen päädytään, mutta laajoja välivaiheita ei tarvita. CAS-ohjelmia voi hyödyntää tehtävän eri vaiheissa. Merkintätapojen kannalta keskeisiä vaiheita ovat periaatteiden ja lakien sekä lopputuloksen ja johtopäätösten esittäminen. Lopputulokset annetaan lähtöarvojen mukaisella tarkkuudella yksiköineen ja johtopäätökset perustellaan.
Mittaustuloksia ja niistä piirrettyjä kuvaajia hyödynnetään tiedon analysoinnissa ja johtopäätösten tekemisessä. Mittauspisteisiin sovitetaan asianmukainen suora. Mittauspisteiden välisiä arvoja voi interpoloida kuvaajaa silmämääräisesti lukemalla tai sopivalla ohjelmalla. Kuvaajaan merkitään akselien nimet, yksiköt ja asteikko. Kuvaajaan merkitään johtopäätösten kannalta olennaiset kohdat, kuten titrauskäyrän ekvivalenttikohta tai hetkellistä nopeutta laskettaessa kyseinen tangentti.
Essee‐ ja selittävissä vastauksissa tekstiä täydennetään reaktioyhtälöillä, kaavoilla tai piirroksilla. Käsiteltäviä ilmiöitä kuvataan makroskooppisella, mikroskooppisella ja symbolisella tasolla. Vastauksesta ilmenee, että tehtävään liittyvää aineistoa on hyödynnetty, sovellettu, analysoitu ja arvioitu tehtävänannon mukaisesti. Hyvä vastaus on jäsennelty ja sisällöltään johdonmukainen.
Vastaus arvostellaan tehtäväkohtaisten kriteerien mukaisesti. Lähtökohtana ovat vastauksen ansiot, joista kertyy pisteitä. Jos keskeinen kemiallinen periaate puuttuu tai se on virheellinen, pisteiden kertyminen päättyy. Tällöin virheellisen tuloksen siirtymistä eteenpäin ei hyväksytä (ei-VSE). Tällaiset virheet ovat esimerkiksi stoikiometriavirheet, väärä rajoittava tekijä tai väärä aine reaktioyhtälössä. Muiden puutteiden tai virheiden tapauksessa virheellisen tuloksen siirtyminen eteenpäin hyväksytään (VSE), jolloin pisteiden kertyminen jatkuu puutteen tai virheen jälkeen. Kokeen osan 3 vaativat tehtävät edellyttävät täsmällisempää periaatteiden hallintaa kuin kokeen alkupään perustehtävät. Kemian kannalta epätäsmällisestä kielenkäytöstä, pienestä laskuvirheestä tai likiarvojen huolimattomasta käytöstä vähennetään 0–3 p. esimerkiksi seuraavasti:
- pyöristys- ja kopiointivirheet, jotka eivät vaikuta lopputulokseen, −0 p.
- kopiontivirheet, pyöristysvirheet ja pienet huolimattomuusvirheet, jotka vaikuttavat lopputulokseen, yksittäinen pieni virhe rakennekaavassa −1 p.
- yksikönmuunnosvirheet, systemaattinen virhe rakennekaavassa tai muut vähäistä suuremmat virheet, jossa ei kuitenkaan ole väärä kemiallinen periaate −2 p.
Osa 1: 20 pisteen tehtävä
1. Monivalintatehtäviä kemian eri osa-alueilta 20 p.
1.1 Hiilivedyn täydellisen palamisreaktion tuotteet ovat 2 p.
- CO₂ ja H₂O. (2 p.)
1.2 Suodatuksessa erottuvat toisistaan 2 p.
- saostuma ja suodos. (2 p.)
1.3 Erään aineen sulamispiste normaalissa ilmanpaineessa on −78,5 ℃ ja kiehumispiste 142 ℃. Tämä aine on todennäköisimmin 2 p.
- molekyyliyhdiste. (2 p.)
1.4 Reaktio 4HCl(g) + O₂(g) ⇌ 2Cl₂(g) + 2H₂O(g) on endoterminen vasemmalta oikealle. Millä keinolla saadaan tasapainoasemaa siirtymään oikealle tuotteiden suuntaan? 2 p.
- Nostetaan painetta. (2 p.)
1.5 Mikä seuraavista kuvauksista sopii erääseen kloorin isotooppiin? 2 p.
- Protonien lukumäärä on 17 ja neutronien lukumäärä 20. (2 p.)
1.6 Missä seuraavista yhdisteistä on vahvin hiili-hiilisidos? 2 p.
- etyynissä (2 p.)
1.7 Mikä seuraavista alkuaineista muodostaa helpoiten kationeja? 2 p.
- Rb (2 p.)
1.8 Kuinka monessa erilaisessa kemiallisessa ympäristössä on vety-ytimiä propan-1-olin ¹H-NMR-spektrissä? 2 p.
- neljässä (2 p.)
1.9 Hiilimonoksidin IR-spektrin piikki kuvaa 2 p.
- hiili-happisidoksen värähdysenergiaa. (2 p.)
1.10 Mikä seuraavista on butan-2-olin isomeeri? 2 p.
- dietyylieetteri (2 p.)
Osa 2: 15 pisteen tehtävät
2. Kemiallinen tasapaino 15 p.
2.1 Happo-emästasapaino 4 p.
2.1.1 1 p.
- protonin (1 p.)
- vetyionin (1 p.)
2.1.2 1 p.
- oksoniumioni (1 p.)
- vetyioni (1 p.)
2.1.3 1 p.
- 7,00 (1 p.)
2.1.4 1 p.
- 7,47 (1 p.)
2.2 Puskuriliuos 3 p.
2.2.1 1 p.
- happamuuden (1 p.)
- pH-arvon (1 p.)
- emäksisyyden (1 p.)
2.2.2 1 p.
- vastinhappoa (1 p.)
- konjugoitua happoa (1 p.)
- konjugaattihappoa (1 p.)
2.2.3 1 p.
- hiilihapon (1 p.)
- hiilidioksidin (1 p.)
2.3 Titraus 3 p.
2.3.1 1 p.
- neutralointireaktioksi (1 p.)
- happo-emäsreaktioksi (1 p.)
- protoninsiirtoreaktioksi (1 p.)
2.3.2 1 p.
- natriumasetaattia (1 p.)
- natriumetanaattia (1 p.)
- asetaattia (1 p.)
- etanaattia (1 p.)
- suolaa (1 p.)
2.3.3 1 p.
- korkeampi (1 p.)
2.4 Kemiallinen tasapaino 5 p.
Valitse oikea vastausvaihtoehto. Jos olet aloittanut tehtävään vastaamisen, mutta et haluakaan jättää tehtävää arvosteltavaksi, poista vastauksesi valitsemalla pudotusvalikosta tyhjä rivi.
Kuvaajassa esitetään erään reaktion aineiden A, B, C ja D konsentraatiot (mol/l) ajan (s) funktiona.
2.4.1 1 p.
- A ja B (1 p.)
2.4.2 1 p.
- x (1 p.)
2.4.3 1 p.
- w (1 p.)
2.4.4 1 p.
- 3 (1 p.)
2.4.5 1 p.
- 1 (1 p.)
Myös muut oikeat ilmaisut hyväksytään.
Tämä tehtävä arvostellaan lautakunnassa keskitetysti, joten opettaja ei tee alustavaa arvostelua. Keskitetysti arvosteltavan vastauksen pisteet päivittyvät arvostelupalveluun lopullisen arvostelun edetessä. Vastauksen kohdalla näkyy arvostelupalvelussa viiva (-), kunnes kyseinen vastaus on arvosteltu.
3. Kuparisulfaattiliuoksen ja sinkin reaktio 15 p.
Sininen kuparisulfaatin vesiliuos ja sinkki reagoivat seuraavan reaktioyhtälön mukaisesti:
CuSO₄(aq) + Zn(s) → Cu(s) + ZnSO₄(aq)
3.1
Eräässä kokeessa kuparisulfaattiliuoksen tilavuus oli 200,0 ml ja konsentraatio 0,683 mol/l. Metallisen sinkin massa oli 1,85 g. Oletetaan, että reaktio tapahtuu kokonaan. Kuinka monta grammaa kuparia voi muodostua kokeessa?
Kuparia saatiin tehdyssä kokeessa 1,066 g. Laske kuparin saantoprosentti.
9 p.
n(CuSO₄) = c · V = 0,683 mol/l · 0,2000 l = 0,1366 mol
n(Zn) = m/M = 1,85 g/(65,38 g/mol) = 0,028296 mol
(1 p.)
Sinkki kuluu loppuun reaktiossa, koska sinkin ainemäärä on pienempi kuin kuparisulfaatin ainemäärä ja reaktioyhtälön kertoimet ovat samat.
(2 p.)
Reaktioyhtälön kertoimien perusteella muodostuneen kuparin ainemäärä on n(Cu) = n(Zn)
(1 p.)
m(Cu) = n · M = 0,028296 mol · 63,55 g/mol = 1,7982 g
(1 p.)
Kuparia muodostuu 1,80 g.
(1 p.)
Kuparin saantoprosentti = 1,066 g / 1,7982 g = 0,59281
(2 p.)
Kuparin saantoprosentti oli 59,3 % (0,593).
(1 p.)
3.2 Mitä havaintoja voit tehdä reaktion aikana? Mainitse kolme reaktioon liittyvää havaintoa. 3 p.
1 p./havainto, esimerkiksi:
- Harmaa metalli/sinkki syöpyy.
- (Kuparisulfaatti)liuoksen (sininen) väri haalenee hieman.
- Punertavaa metallia/kuparia muodostuu harmaan metallin/sinkin pinnalle ja astian pohjalle.
3.3 Onko reaktio hapettumis-pelkistymisreaktio? Perustele vastauksesi hapetuslukujen (hapetusasteiden) avulla. 3 p.
Reagoivien aineiden hapetusluvut:
| lähtöaine | reaktiotuote | |
|---|---|---|
| Cu | +2 | 0 |
| Zn | 0 | +2 |
(2 p.)
Koska reagoivien aineiden hapetusluvut muuttuvat, reaktio on hapettumis-pelkistymisreaktio. (1 p.)
4. Fingolimodin synteesi 15 p.
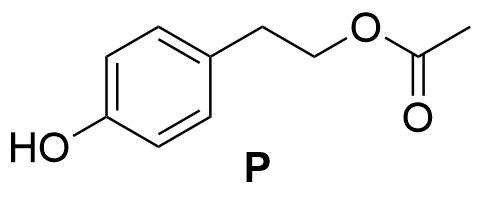
4.1 Synteesin ensimmäisessä vaiheessa käytetään menetelmää, jossa ainoastaan yhdisteen O primäärinen hydroksiryhmä reagoi etikkahapon kanssa. Tällöin syntyy välituote P, joka on esteri. Piirrä välituotteen P rakennekaava. Voit hyödyntää vastauksessasi tiedostoa . 3 p.
4.2 Fingolimodin (Q) massaprosenttinen koostumus on seuraava: 74,22 % hiiltä, 10,82 % vetyä, 4,556 % typpeä ja 10,41 % happea. Kuinka monta hiiliatomia on hiilivetyketjussa, joka on merkitty fingolimodin rakennekaavaan kirjaimella R? 7 p.
Tehtävän voi ratkaista hyvin monella eri tavalla. Alla on esitetty yksi tapa.
Oletetaan fingolimodia olevan 100 g, jolloin
m(N) = 4,556 g, m(C) = 74,22 g, m(H) = 10,82 g ja m(O) = 10,41 g.
(1 p.)
Tällöin ainemäärät ovat:
n(N) = m(N) / M(N) = 4,556 g / 14,01 g/mol = 0,325196 mol
n(C) = m(C) / M(C) = 74,22 g / 12,01 g/mol = 6,17985 mol
n(H) = m(H) / M(H) = 10,82 g / 1,008 g/mol = 10,734127 mol
n(O) = m(O) / M(O) = 10,41 g / 16,00 g/mol = 0,650625 mol
(2 p.)
Määritetään fingolimodin suhdekaava:
N: 1
C: n(C) / n(N) = 6,17985 mol / 0,325196 mol = 19,0034 ≈ 19
H: n(H) / n(N) = 10,73413 mol / 0,325196 mol = 33,0081 ≈ 33
O: n(O) / n(N) = 0,650625 mol / 0,325196 mol = 2,00071 ≈ 2
(C₁₉H₃₃NO₂)ₓ
(1 p.)
Koska ketju koostuu ainoastaan hiilestä ja vedystä, on fingolimodissa ainoastaan yksi typpiatomi. Tästä seuraa, että fingolimodin molekyylikaava on C₁₉H₃₃NO₂.
(1 p.)
Rakenteen Q perusteella hiiliatomeja on muualla kuin ketjussa R yhteensä 11,
(1 p.)
josta saadaan laskettua ketjun R hiiliatomien määrä:
19 − 11 = 8.
(1 p.)
4.3 Miten fingolimodin (Q) vesiliukoisuus pH-arvossa 1 eroaa sen vesiliukoisuudesta pH-arvossa 13? Perustele vastauksesi. 5 p.
Kun pH on 1, vesiliuos on voimakkaasti hapan. Tällöin fingolimodin aminoryhmä on vastaanottanut protonin / vetyionin eli se on happomuodossaan (-\mathrm{NH_3^+}). Vastaavasti, kun pH on 13, vesiliuos on voimakkaasti emäksinen. Tällöin fingolimodin aminoryhmä on emäsmuodossaan (-\mathrm{NH_2}) eli se ei ole vastaanottanut tai luovuttanut protonia / vetyionia. (2 p.)
Vesimolekyyli pystyy muodostamaan ioni-dipolisidoksia positiivisesti varautuneen aminoryhmän (happomuoto) kanssa. Vesimolekyyli muodostaa vetysidoksia (emäsmuodon) aminoryhmän kanssa, jossa on vain osittaisvarauksia. Ioni-dipolisidokset ovat vahvempia kuin vetysidokset. (2 p.)
Tämän takia fingolimodi liukenee paremmin happamaan kuin emäksiseen vesiliuokseen. (1 p.)
5. Ammoniumkloridin puhtauden määritys 15 p.
5.1 Kirjoita kaikki työhön liittyvät reaktioyhtälöt. 6 p.
Ammoniumkloridin reaktio natriumhydroksidin kanssa keitettäessä:
NH₄Cl(s/aq) + NaOH(aq) → NH₃(g/aq) + NaCl(aq) + H₂O(l)
(2 p.)
Vapautuneen ammoniakin reaktio vetykloridiliuoksen kanssa:
\mathrm{NH_3(g/aq)+HCl(aq)}\rightarrow\mathrm{NH_4^+(aq)+Cl^-(aq)}
(2 p.)
Vetykloridihapon reaktio titrauksessa natriumhydroksidin kanssa:
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
(2 p.)
5.2 Laske ammoniumkloridin puhtaus massaprosentteina. 7 p.
Vetykloridin kokonaisainemäärä:
n(HCl)kok. = c · V = 0,100 l · 0,1013 mol/l = 10,130 · 10⁻³ mol
(1 p.)
Titratun vetykloridin ainemäärä:
n(HCl)ylim. = n(NaOH)titr. = c · V = 0,1925 mol/l · 0,00712 l = 1,3706 ·10⁻³ mol
(1 p.)
Ammoniumkloridin ainemäärä:
n(NH₄Cl) = n(HCl)kok. − n(HCl)ylim. = 10,130 · 10⁻³ mol − 1,3706 ·10⁻³ mol = 8,7594 ·10⁻³ mol
(2 p.)
Ammoniumkloridin massa ja puhtaus:
m(NH₄Cl) = n · M = 8,7594 ·10⁻³ mol · 53,492 g/mol = 0,468558 g
(1 p.)
Puhtaus massaprosentteina = m(NH₄Cl)/m(näyte) · 100 % = 0,46856 g / 0,5086 · 100 % = 92,12698 % = 92,1 %
(2 p.)
5.3 Miksi oli tärkeää, että reaktiot tehtiin vetokaapissa? 2 p.
Reaktiossa vapautuu ammoniakkikaasua, joka on voimakkaan hajuista ja hengitettäessä voimakkaasti ärsyttävää. Vaikka ammoniakki imeytetään happamaan vesiliuokseen, on tarpeen varmistaa, ettei ammoniakki missään tilanteessa pääse hengitysilmaan.
6. Indigokarmiini 15 p.
6.1 Tarkastellaan indigokarmiinin muotoa A. Molekyylin päissä ovat natriumsulfonaattiryhmät –SO₃Na. Nimeä muut indigokarmiinin muodon A funktionaaliset ryhmät. 4 p.
Oikeat ryhmät, 1.p./ryhmä, korkeintaan 4 p.:
- aminoryhmä
- hydroksiryhmä
- karbonyyliryhmä
- hiiliatomien välinen kaksoissidos
- aromaattinen rengas / fenyyliryhmä
6.2 Mikä indigokarmiinin muodoista A, B ja C on hapettunein? Perustele vastauksesi indigokarmiinin rakenteen avulla. 4 p.
Hapettunein muoto on B. (2 p.)
Perustelu (esimerkiksi): Muodossa B hapen suhteellinen osuus yhdisteessä on suurin. (2 p.)
6.3 Videolla vesiliuos kaadetaan toiseen keitinlasiin, jolloin indigokarmiini hapettuu. Mikä aiheuttaa indigokarmiinin hapettumisen? Vastausta ei tarvitse perustella. 2 p.
Ilman happi aiheuttaa indigokarmiinin hapettumisen.
6.4 Millä muulla tavalla kuin kaatamalla vesiliuoksen toiseen keitinlasiin voisit hapettaa vesiliuoksessa olevan indigokarmiinin? Mainitse yksi tapa. 2 p.
Vastauksessa on mainittu yksi tapa, esimerkiksi jokin seuraavista:
- Liuosta voidaan sekoittaa tai ravistella.
- Liuokseen voidaan johtaa happea.
- Liuokseen voidaan lisätä hapetinta / hapettavaa ainetta.
6.5 Glukoosi saa aikaan indigokarmiinin pelkistymisen. Ohessa on esitelty glukoosin rakennekaava. Miksi glukoosi voi toimia pelkistimenä? Perustele vastauksesi glukoosimolekyylin rakenteen avulla. 3 p.
Glukoosissa on funktionaalisia ryhmiä, jotka voivat itse hapettua ja siten pelkistää indigokarmiinin. (1 p.)
Esimerkkejä näistä ryhmistä:
- (Primäärinen) hydroksiryhmä voi hapettua aldehydiksi.
- (Sekundäärinen) hydroksiryhmä voi hapettua ketoniksi.
- Aldehydiryhmä voi hapettua karboksyylihapoksi.
(2 p.)
7. Typpitrikloridin tasapaino 15 p.
Typpitrikloridi NCl₃ on erittäin helposti räjähtävä yhdiste. Suljetussa astiassa typpitrikloridi muodostaa tasapainotilan hajoamistuotteidensa kanssa seuraavasti:
2NCl₃(g) ⇌ N₂(g) + 3Cl₂(g)
Reaktion tasapainovakio on 3,3 · 10⁻¹² (mol²/l²).
7.1 Tuntematon määrä kaasumaista typpitrikloridia suljettiin astiaan, jonka tilavuus oli 2,0 l. Kun tasapainotila oli saavutettu, typen konsentraatioksi astiassa määritettiin 3,2 · 10⁻⁶ mol/l. Kuinka monta milligrammaa typpitrikloridia suljettiin astiaan alun perin? 8 p.
c = 3,2 · 10⁻⁶ mol/l
K = 3,3 · 10⁻¹²
M(NCl₃) = 14,01 g/mol + 3 · 35,45 g/mol = 120,36 g/mol
V = 2,0 l
Tasapainotarkastelu:
| 2NCl₃(g) | ⇌ | N₂(g) | + | 3Cl₂(g) | |
|---|---|---|---|---|---|
| Alussa | x | 0 | 0 | ||
| Muutos | −2c | +c | +3c | ||
| Tasapainossa | x − 2c | c | 3c |
(2 p.)
K = [N₂][Cl₂]³ / [NCl₃]²
(1 p.)
= c · (3 · c)³ / (x − 2c)²
(1 p.)
Ratkaistaan x:
x = \pm\sqrt{\frac{27c^4}{K}} + 2c
= 3,569037 · 10⁻⁵ mol/l (tai x = −2,289037 · 10⁻⁵ mol/l)
(1 p.)
Ratkaistaan typpitrikloridin massa alussa:
n = x · V
m = n · M(NCl₃) = x · V · M(NCl₃) = 3,569037 · 10⁻⁵ mol/l · 2,0 l · 120,36 g/mol
= 0,008591386 g
= 8,6 mg
(3 p.)
7.2 Typpitrikloridin hajoamisreaktio suljetussa astiassa on tasapainoreaktio. Miksi reaktio on yksisuuntainen avoimessa tilassa? 3 p.
Avoimessa tilassa tuotteet leviävät ympäristöön. (1 p.)
Näin ollen hajoamisreaktion käänteisreaktiota ei voi tapahtua merkittävissä määrin (1 p.) eikä systeemi saavuta tasapainotilaa. (1 p.)
TAI
Avoimessa tilassa tuotteet leviävät ympäristöön. (1 p.)
Tuotteita poistuu reaktioyhtälön oikealta puolelta (1 p.), jolloin tasapainoasema siirtyy jatkuvasti kohti tuotteita eikä reaktio saavuta koskaan tasapainotilaa. (1 p.)
7.3 Typpitrikloridin muodostumisentalpia on 232 kJ/mol. Miten lämpötilan nostaminen vaikuttaa typpitrikloridin hajoamisreaktion tasapainoasemaan? Perustele vastauksesi. 4 p.
Typpitrikloridin hajoamisreaktio on sen muodostumisreaktion käänteisreaktio. Näin ollen käänteisreaktion reaktioentalpia on muodostumisentalpian vastaluku eli −232 kJ/mol. (2 p.)
Hajoamisreaktio on siis eksoterminen. (1 p.)
Näin ollen lämpötilan kasvattaminen siirtää tasapainoasemaa lähtöaineiden suuntaan. (1 p.)
8. Hiilivetyjen orbitaalit 15 p.
8.1
Valitse oikea hybridisaatio. Oikea vastaus 1 p., väärä vastaus 0 p., ei vastausta 0 p.
Jos olet aloittanut tehtävään vastaamisen, mutta et haluakaan jättää tehtävää arvosteltavaksi, poista vastauksesi valitsemalla pudotusvalikosta tyhjä rivi.
3 p.
8.1.1 Mikä on etaanin hiiliatomien hybridisaatio? 1 p.
- sp³ (1 p.)
8.1.2 Mikä on eteenin hiiliatomien hybridisaatio? 1 p.
- sp² (1 p.)
8.1.3 Mikä on etyynin hiiliatomien hybridisaatio? 1 p.
- sp (1 p.)
8.2 Esiintyykö eteenillä H₂C=CH₂ konformaatioisomeriaa? Perustele vastauksesi orbitaalien avulla. 5 p.
(Eteenissä hiiliatomit ovat sp²-hybridisoituneet.) C–C-sidoksen muodostumiseen osallistuu kaksi sp²-hybridiorbitaalia sekä kaksi molekyylin tasoon nähden kohtisuoraa p-orbitaalia. (1 p.)
Orbitaaleista muodostuu yksi σ-sidos ja yksi π-sidos. (1 p.)
π-sidos ei voi vapaasti kiertyä. Tämä estää CH₂-ryhmien vapaan kiertymisen C=C-kaksoissidoksen ympäri. (2 p.)
Näin ollen eteenillä ei esiinny konformaatioisomeriaa. (1 p.)
8.3 Bentsoehapon rakennekaava on esitetty ohessa. Bentsoehapon kaikkien hiiliatomien hybridisaatio on sp². Mitä tämän perusteella voidaan päätellä sen kolmiulotteisesta rakenteesta? Perustele vastauksesi. 3 p.
sp²-hybridisoituneet hiilet muodostavat tasomaisen rakenteen. Tästä voimme päätellä, että bentseenirengas on tasomainen. Karboksyylihapporyhmän hiili, kaksi happiatomia ja bentseenirenkaan hiiliatomi, johon karboksyyliryhmä sitoutuu, ovat keskenään samassa tasossa. Hydroksiryhmän vedyn asentoa emme voi päätellä hiiliatomien hybridisaatiosta.
8.4 Perustele bentseenin orbitaalirakenteen avulla, miksi sen kaikki kuusi hiili-hiilisidosta ovat yhtä pitkiä. 4 p.
(Hiiliatomit ovat sp²-hybridisoituneet.) Jokaisen vierekkäisen hiiliatomin välissä on samanlainen σ-sidos. (1 p.)
Molekyylin tasoon nähden kohtisuorat kuusi p-orbitaalia yhdistyvät, (1 p.)
jolloin muodostuu π-sidos, joka on delokalisoitunut koko renkaan ympäri. (2 p.)
(Näin ollen kaikki hiili-hiilisidokset ovat identtisiä.)
Osa 3: 20 pisteen tehtävät
9. Telluurin tuotanto 20 p.
Telluuri on hopeanharmaa puolimetalli, jota käytetään muun muassa aurinkokennoissa. Sillä on samankaltaisia kemiallisia ominaisuuksia kuin rikillä.
Telluuria esiintyy muun muassa kuparimalmin seassa kupari(I)telluridina Cu₂Te. Kuparin jalostamisen yhteydessä kupari(I)telluridia kertyy kuparin elektrolyysin sivutuotteena muodostuvaan liejuun. Telluuria tuotetaan tästä elektrolyysin sivutuotteesta monivaiheisella prosessilla.
9.1
Telluurin erotusprosessin ensimmäisessä vaiheessa kupari(I)telluridia kuumennetaan natriumkarbonaatin kanssa lämpötilassa 500 ℃. Kupari(I)telluridi reagoi natriumkarbonaatin ja ilman hapen kanssa muodostaen kiinteää natriumtelluriittia Na₂TeO₃ ja metallista kuparia. Reaktiossa vapautuu hiilidioksidia.
Kirjoita tätä prosessin vaihetta kuvaava reaktioyhtälö.
3 p.
Cu₂Te(s) + O₂(g) + Na₂CO₃(s) → Na₂TeO₃(s) + 2Cu(s) + CO₂(g)
- Kaikki aineet ovat oikein. (1 p.)
- Lisäksi kaikki kertoimet ovat oikein (1 p.) ja kaikki olomuodot ovat oikein (1 p.).
9.2 Mitä ympäristövaikutuksia osatehtävässä 9.1 kuvatulla prosessilla on? Mainitse kolme asiaa. 3 p.
Esimerkiksi kolme seuraavista ympäristövaikutuksista (1 p./esimerkki):
- Suhteellisen korkea lämpötila vaatii energiaa. Ympäristövaikutukset riippuvat käytetystä energialähteestä. Esimerkiksi, jos energia tuotetaan fossiilisilla polttoaineilla, siitä aiheutuu hiilidioksidipäästöjä.
- Tuotteena syntyvä hiilidioksidi on kasvihuonekaasu.
- Lähtöaineena käytetyn natriumkarbonaatin tuottaminen kuluttaa energiaa ja raaka-aineita.
- Telluuriyhdisteet (ovat lievästi myrkyllisiä, ja ne) on otettava prosessissa huolellisesti talteen, eikä niitä saa päästää ympäristöön.
9.3
Erotusprosessin seuraavassa vaiheessa natriumtelluriitti Na₂TeO₃ liuotetaan veteen, jolloin natriumtelluriitti saadaan erotettua metallisesta kuparista.
Telluriitti-ioni \mathrm{TeO}_3^{2-} on emäs. Sen vastinhappo on vetytelluriitti-ioni \mathrm{HTeO}_3^{-}, jonka happovakion arvo on 2,3 · 10⁻³ (mol/l).
Kirjoita telluriitti-ionin protoninsiirtoreaktion reaktioyhtälö.
4 p.
\mathrm{TeO_3^{2-}(aq)}+\mathrm{H_2O(l)}\xrightleftharpoons{ }\ \mathrm{HTeO_3^-(aq)}+\mathrm{OH^-(aq)}
TAI
Na₂TeO₃(aq) + H₂O(l) ⇌ NaHTeO₃(aq) + NaOH(aq)
- Kaikki aineet ovat oikein. (1 p.)
- Lisäksi kaikki kertoimet ovat oikein (2 p.) ja kaikki olomuodot ovat oikein (1 p.).
9.4
Erotusprosessin seuraavassa vaiheessa natriumvetytelluriitin vesiliuokseen lisätään rikkihappoa, jolloin liuoksesta saostuu telluuridioksidia TeO₂:
2NaHTeO₃(aq) + H₂SO₄(aq) → 2TeO₂(s) + Na₂SO₄(aq) + 2H₂O(l)
Telluuridioksidi TeO₂ voidaan pelkistää elektrolyyttisesti telluuriksi happamasta vesiliuoksesta.
Kirjoita telluuridioksidin elektrolyyttisen pelkistämisen anodi- ja katodireaktioiden sekä kokonaisreaktion reaktioyhtälöt. Oletetaan, että elektrodit ovat inerttejä. Tässä osatehtävässä reaktioihin ei tarvitse merkitä olomuotoja.
6 p.Anodi:
2H₂O → O₂ + 4H⁺ + 4e⁻
(2 p.)
Katodi:
TeO₂ + 4H⁺ + 4e⁻ → Te + 2H₂O
(2 p.)
Kokonaisreaktio:
TeO₂ → Te + O₂
(2 p.)
9.5
Osatehtävässä 9.4 kuvatun elektrolyysin sijasta telluuridioksidin voi pelkistää myös reaktiolla, jossa kaasumaista rikkidioksidia johdetaan telluuridioksidin ja rikkihapon seokseen:
TeO₂(s) + 2SO₂(g) + 2H₂O(l) → Te(s) + 2H₂SO₄(aq)
Tarkastellaan sekä rikkidioksidiin että osatehtävässä 9.4 kuvattuun elektrolyysiin perustuvia pelkistysprosesseja. Mitä näissä prosesseissa pitäisi huomioida, jotta telluurin tuotanto olisi mahdollisimman ympäristöystävällistä?
4 p.Elektrolyysillä pelkistäminen, 1 p./huomio, enintään 2 p. Esimerkkejä huomioista:
- Elektrolyysi vaatii runsaasti sähköenergiaa, ja tämä tulee tuottaa käyttäen uusiutuvia energialähteitä ympäristövaikutusten minimoimiseksi.
- (Telluuri on lievästi myrkyllistä.) Se on otettava prosessissa huolellisesti talteen, eikä sitä saa päästää ympäristöön.
Rikkidioksidilla pelkistäminen, 1 p./huomio, enintään 3 p. Esimerkkejä huomioista:
- Rikkidioksidin tuottaminen vaatii energiaa.
- Kaasumaista rikkidioksidia ei saa vapautua ympäristöön.
- Rikkidioksidin vesiliuos on syövyttävää ja haitallista vesieliöille, joten sitä ei saa päästä ympäristöön.
- Sivutuotteena muodostuva rikkihappo pitää pystyä ottamaan talteen ja käyttämään uudelleen.
10. Reaktionopeus ja aktivaatioenergia 20 p.
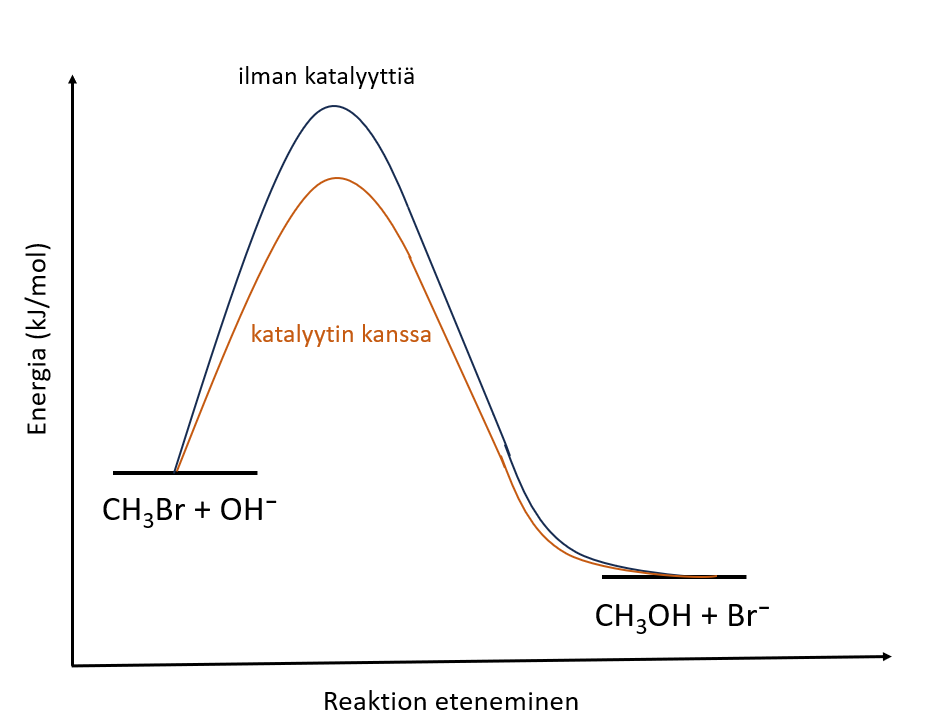
10.1 Onko kuvaajassa kuvattu bromimetaanin ja hydroksidi-ionin välinen reaktio endoterminen vai eksoterminen? Perustele vastauksesi. 3 p.
Reaktio on eksoterminen. (1 p.)
Reaktiossa vapautuu energiaa, koska lähtöaineiden energia on suurempi kuin tuotteiden (tai tuotteiden energia on alhaisempi kuin lähtöaineiden). (2 p.)
10.2 Miten katalyytti vaikuttaisi kuvaajassa esitetyn reaktion etenemiseen? Esitä vastauksesi yhtenä kuvana. Ota kuvaajasta kuvakaappaus tai tallenna se kuvana. Piirrä kuvaajaan piirto-ohjelmalla lisäykset, jotka kuvaavat reaktion etenemistä, kun käytetään katalyyttiä. Liitä vastaukseen kuvakaappaus laatimastasi täydennetystä kuvasta. 4 p.
10.3 Metanolia voidaan tuottaa hiilidioksidin ja vedyn välisen reaktion avulla. Teollisessa tuotannossa reaktiota tehostetaan lisäämällä reaktiokammioon katalyyttiä. Suunnittele tutkimus, jossa tutkitaan kahden erilaisen katalyytin vaikutusta reaktionopeuteen. Kuvaile tutkimuksen suorittaminen, siinä tehtävät mittaukset ja vakioina pidettävät tekijät. 5 p.
Suoritetaan kaksi erillistä koetta; yhdessä kokeessa katalyyttinä on A ja toisessa B. Kummassakin kokeessa mitataan jommankumman lähtöaineen tai tuotteen konsentraation muutosta. (2 p.)
Muutos mitataan kummassakin kokeessa yhtä pitkän ajan kuluttua. (1 p.)
Lämpötila ja lähtöaineiden alkupitoisuudet / (osa)paineet pidetään vakiona. (2 p.)
10.4
Vetyjodidin hajoamisreaktion (2HI → H₂ + I₂) aktivaatioenergia on 179 kJ/mol. Lämpötilassa 573 K reaktionopeuskertoimen luonnollisen logaritmin arvo on ln(k) = −12,747. Mikä aktivaatioenergian arvon pitäisi olla, jotta reaktionopeuskertoimen arvo kaksinkertaistuisi lämpötilassa 573 K?
ln(2k) = −12,054
8 p.
Merkitään seuraavasti: nopeusvakiota k₁ vastaava aktivaatioenergia on Eₐ₁ ja nopeusvakiota k₂ vastaava aktiovaatioenergia on Eₐ₂
ln(k₁) = ln(A) − Eₐ₁/(RT)
ln(k₂) = ln(2k₁) = ln(A) − Eₐ₂/(RT)
(2 p.)
ln(k₁) − ln(2k₁) = Eₐ₂/(RT) − Eₐ₁/(RT)
Eₐ₂/(RT) = ln(k₁) − ln(2k₁) + Eₐ₁/(RT)
(3 p.)
Eₐ₂ = RT(ln(k₁) − ln(2k₁)) + Eₐ₁
= 8,314463 J/(K mol) · 573 K (−12,747 − (−12,054)) + 179 000 J/mol
= 175 698,42 J/mol
= 176 kJ/mol
(3 p.)
11. Amiinien reaktioita 20 p.
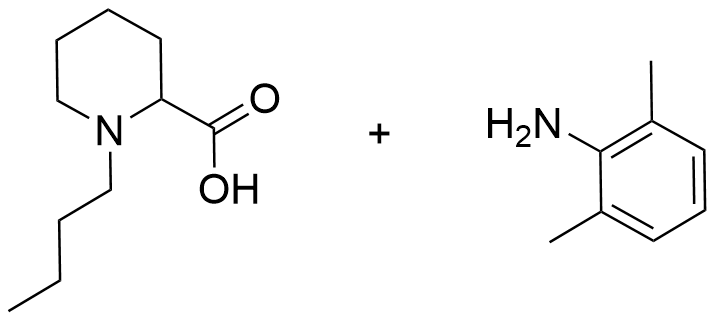
11.1 Piirrä reaktion A tuotteiden rakennekaavat. Voit hyödyntää vastauksessasi tiedostossa annettua bupivakaiinin rakennekaavaa. 4 p.
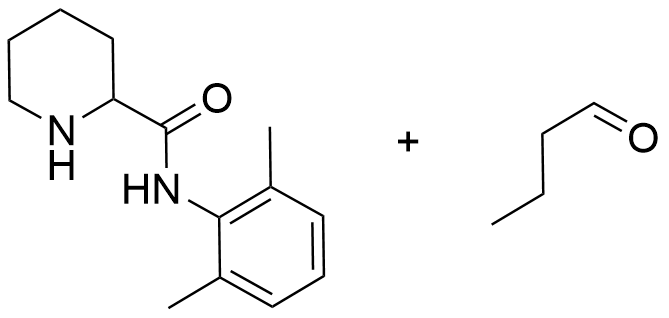
11.2 Piirrä reaktion B tuotteiden rakennekaavat. Voit hyödyntää vastauksessasi tiedostossa annettua bupivakaiinin rakennekaavaa. 4 p.
11.3
Kun erästä kaasumaista amiinia (CxHyNz) poltettiin, reaktiotuotteina syntyi hiilidioksidia (CO2), typpeä (N2) ja vettä (H2O). Amiinin palamisreaktio on
2CxHyNz(g) + (4x + y)/2O2(g) → 2xCO2(g) + zN2(g) + yH2O(g).
Reaktion lähtöaineena oli 10,0 ml amiinia. Kun reaktiotuotteena saatu kaasuseos jäähdytettiin huoneen lämpötilaan, kaasuseoksesta oli poistunut 25,0 millilitraa kaasua. Tilavuuden pieneneminen johtui yhden reaktiotuotteen olomuodon muutoksesta. Kun kaasuseos tämän jälkeen pestiin emäksisellä pesuliuoksella, kaasuseoksesta poistui 10,0 ml kaasua. Lopulta pesun jälkeen jäljellä oli 5,0 ml kaasua. Kaikki tilavuudet mitattiin huoneenlämpötilassa.
Päättele annettujen tietojen perusteella kertoimet x, y ja z. Perustele vastauksesi.
Esitä vastauksessasi tasapainotettu reaktioyhtälö ja nimeä lähtöaineena käytetty amiini.
Ilmankosteutta ja veden höyrynpainetta ei huomioida. Kaikki kaasut oletetaan ideaalikaasuiksi. Ideaalikaasujen tilavuudet ovat suoraan verrannollisia niiden ainemääriin.
12 p.2CxHyNz(g) + (4x + y)/2O₂(g) → 2xCO₂(g) + zN₂(g) + yH₂O(g)
Reaktiossa oli vain kaasuja, joten stoikiometriset kertoimet ilmaisevat reagoivien aineiden ainemäärä- ja tilavuussuhteet.
Kertoimen y päättely:
Kun seos jäähdytettiin huoneen lämpötilaan, vesihöyry tiivistyi nesteeksi eli se poistui kaasuseoksesta. Vesihöyryä oli 25,0 ml.
(1 p.)
Vesihöyryä on amiiniin nähden 25,0 ml/10 ml eli 2,5-kertainen määrä. Siten veden kerroin y = 2 · 2,5 = 5.
(2 p.)
Kertoimen x päättely:
Jäljelle jääneessä kaasuseoksessa oli hiilidioksidia ja typpeä. Hiilidioksidi poistui emäksiseen pesuliuokseen. Hiilidioksidia oli siten 10,0 ml.
(1 p.)
Koska amiinia oli 10 ml ja hiilidioksidia muodostui 10 ml, kerroin x = 1.
(1 p.)
Nyt saadaan hapen kerroin (4x + y)/2 = (4 · 1 + 5)/2 = 4,5.
(2 p.)
Kertoimen z päättely:
Pesun jälkeen jäljellä oli vain typpikaasua (5,0 ml).
(1 p.)
Koska amiinia oli lähtöaineena 10,0 ml ja typpeä muodostui 5 ml, z =1.
(2 p.)
Näin saadaan reaktioyhtälön kertoimet:
2CH₅N(g) + 4,5O₂(g) → 2CO₂(g) + N₂(g) + 5H₂O(g).
Kerrotaan kertoimet kahdella, jotta saadaan kokonaislukukerroin hapelle:
4CH₅N(g) + 9O₂(g) → 4CO₂(g) + 2N₂(g) + 10H₂O(g).
(1 p.)
Yhdiste on metyyliamiini/metaaniamiini.
(1 p.)