Beskrivningar av goda svar: SV – Kemi
20.3.2026
Preliminära beskrivningar av goda svar 20.3.2026
De preliminära beskrivningarna av goda svar utgör en riktgivande beskrivning av de svar som förväntas på uppgifterna i provet. De är i första hand ämnade som stöd för den preliminära bedömningen. De preliminära beskrivningarna av goda svar innehåller och beskriver inte nödvändigtvis alla godkända svar. De preliminära beskrivningarna av goda svar utgör inte en del av den uppgift om hur bedömningsgrunderna tillämpats på en enskild examinands provprestation som avses i Studentexamensnämndens allmänna föreskrifter och anvisningar. De preliminära beskrivningarna av goda svar är inte bindande för Studentexamensnämnden då grunderna för den slutgiltiga bedömningen fastställs.
Med studentexamensprovet utreds om studerandena tillägnat sig de kunskaper och färdigheter som anges i gymnasiets läroplan och uppnått tillräcklig mognad enligt målen för gymnasieutbildningen. Målet för bedömningen i läroämnet kemi är en förståelse för och en tillämpning av den kemiska kunskapen. Vid bedömningen beaktas även de färdigheter med vilka man tillägnar sig experimentell kunskap och förmågan att behandla den. Till sådan kunskap hör till exempel planering av experiment, trygg hantering av arbetsredskap och reagens, presentation och tolkning av resultat samt förmågan att dra slutsatser och tillämpa dem.
Vid bedömningen av uppgifterna i kemi läggs vikten vid ett framställningssätt som betonar läroämnets karaktär och vid precision i begreppen och språkbruket. Reaktionsformlerna ställs upp utan oxidationstal med minsta möjliga heltalskoefficienter och med aggregationstillstånden angivna. I organiska reaktionslikheter används strukturformler, men aggregationstillstånd krävs inte. Olika sätt att skriva strukturformler godkänns.
I beräkningsuppgifter ska storhetsekvationer och formler användas på ett sätt som visar att examinanden förstått uppgiften rätt och tillämpat korrekt princip eller lag i sin lösning. Av svaret framgår entydigt hur man når slutresultatet, men omfattande mellansteg behövs inte. CAS-program kan utnyttjas i uppgiftens olika skeden. De principer och lagar som gäller den aktuella situationen samt uppgiftens slutresultat och de slutsatser som dras utgående från lösningen är av central betydelse och ska framgå av svaret. Slutresultaten ges med enheter och med den noggrannhet som utgångsvärdena kräver, och slutsatserna motiveras.
Mätresultat och grafer som ritats utgående från dessa utnyttjas vid analysen av data och då man drar slutsatser. Till mätpunkterna anpassas en vederbörlig rät linje Värden som ligger mellan mätpunkterna kan interpoleras med ögonmått genom visuell avläsning av grafen eller med hjälp av ett lämpligt program. Axlarnas namn, enheter och skala märks ut i grafen. I grafen anges sådana punkter som är väsentliga för slutsatserna, som ekvivalenspunkten för en titrerkurva eller tangenten som används när man beräknar en hastighet vid en given tidpunkt.
I essäsvar och förklarande svar kompletteras texten med reaktionsformler, ekvationer eller teckningar. Fenomenen som behandlas beskrivs på makroskopisk, mikroskopisk och symbolisk nivå. Av svaret framgår att det material som hör ihop med uppgiften har använts, tillämpats, analyserats och utvärderats i enlighet med uppgiftsformuleringen. Ett svar på god nivå är välstrukturerat och innehållsmässigt konsekvent.
Svaren bedöms enligt de kriterier som gäller för respektive uppgift. Utgångspunkten vid bedömningen är de förtjänster för vilka poäng ansamlas. Om en central kemisk princip saknas eller är felaktig avslutas poängansamlingen. Då godkänns inte fortplantning av det felaktiga resultatet (ej-FF). Exempel på sådana fel är stökiometrifel, fel begränsande faktor samt fel ämne i en reaktionslikhet. För övriga brister eller fel godkänns fortplantning av det felaktiga resultatet (FF), och då fortsätter ansamlingen av poäng efter bristfälligheten eller felet. I de krävande uppgifterna i provets del 3 förutsätts en större precision i behandlingen av principer än i de grundläggande uppgifterna i början av provet. Ur kemisk synvinkel inexakt språkbruk, små räknefel eller slarvig användning av närmevärden orsakar avdrag på 0–3 p. till exempel på följande sätt:
- avrundnings- och kopieringsfel som inte påverkar slutresultatet, −0 p.
- kopieringsfel, avrundningsfel och små slarvfel som påverkar slutresultatet, ett enskilt litet fel i en strukturformel, −1 p.
- enhetsomvandlingsfel, systematiska fel i en strukturformel samt övriga fel som till sin natur är allvarligare än små fel, men där det ändå inte är fråga om en felaktig kemisk princip, −2 p.
Del 1: 20-poängsuppgift
1. Flervalsuppgifter från kemins olika delområden 20 p.
1.1 I ett kolvätes fullständiga förbränningsreaktion är produkterna 2 p.
- CO₂ och H₂O. (2 p.)
1.2 I en filtrering separeras 2 p.
- fällningen och filtratet. (2 p.)
1.3 Vid normaltryck har ett visst ämne smältpunkten −78,5 ℃ och kokpunkten 142 ℃. Det är mest sannolikt att det här ämnet är en 2 p.
- molekylförening. (2 p.)
1.4 Reaktionen 4HCl(g) + O₂(g) ⇌ 2Cl₂(g) + 2H₂O(g) är endoterm från vänster till höger. Med vilken åtgärd kan man få jämviktsläget att förskjutas mot höger, alltså mot produkterna? 2 p.
- Genom att höja trycket. (2 p.)
1.5 Vilken av följande beskrivningar passar in på en viss isotop av klor? 2 p.
- Antalet protoner är 17 och antalet neutroner är 20. (2 p.)
1.6 Vilken av följande föreningar har den starkaste kol-kolbindningen? 2 p.
- etyn (2 p.)
1.7 Vilket av följande grundämnen bildar lättast katjoner? 2 p.
- Rb (2 p.)
1.8 I hur många olika kemiska omgivningar förekommer vätekärnor i ¹H-NMR-spektrumet för propan-1-ol? 2 p.
- fyra (2 p.)
1.9 Toppen i IR-spektrumet för kolmonoxid beskriver 2 p.
- vibrationsenergin för kol-syrebindningen. (2 p.)
1.10 Vilket av följande ämnen är en isomer till butan-2-ol? 2 p.
- dietyleter (2 p.)
Del 2: 15-poängsuppgifter
2. Kemisk jämvikt 15 p.
2.1 Syra-basjämvikt 4 p.
2.1.1 1 p.
- en proton (1 p.)
- en vätejon (1 p.)
2.1.2 1 p.
- oxoniumjon (1 p.)
- vätejon (1 p.)
2.1.3 1 p.
- 7,00 (1 p.)
2.1.4 1 p.
- 7,47 (1 p.)
2.2 Buffertlösningar 3 p.
2.2.1 1 p.
- surheten (1 p.)
- pH-värdet (1 p.)
- basiciteten (1 p.)
- basiskheten (1 p.)
2.2.2 1 p.
- konjugerade syra (1 p.)
- konjugatsyra (1 p.)
2.2.3 1 p.
- kolsyra (1 p.)
- koldioxid (1 p.)
2.3 Titrering 3 p.
2.3.1 1 p.
- neutralisationsreaktion (1 p.)
- syra-basreaktion (1 p.)
- protonöverföringsreaktion (1 p.)
2.3.2 1 p.
- natriumacetat (1 p.)
- natriumetanat (1 p.)
- acetat (1 p.)
- etanat (1 p.)
- salt (1 p.)
2.3.3 1 p.
- högre (1 p.)
2.4 Kemisk jämvikt 5 p.
Välj rätt svarsalternativ. Om du har börjat besvara uppgiften men kommer till att du ändå inte vill lämna in den för bedömning kan du radera ditt svar genom att välja den tomma raden i rullgardinsmenyn.
I graf visas koncentrationerna (mol/l) för ämnena A, B, C och D i en viss reaktion som funktion av tiden (s).
2.4.1 1 p.
- A och B (1 p.)
2.4.2 1 p.
- x (1 p.)
2.4.3 1 p.
- w (1 p.)
2.4.4 1 p.
- 3 (1 p.)
2.4.5 1 p.
- 1 (1 p.)
Även andra korrekta uttryck godkänns.
Denna uppgift bedöms centraliserat i nämnden, vilket betyder att läraren inte utför den preliminära bedömningen. Poängen för det centraliserat bedömda svaret uppdateras automatiskt i bedömningstjänsten under censorarbetets gång. Tills svaret i fråga har bedömts märks svaret med ett streck (-) i bedömningstjänsten.
3. Reaktionen mellan en kopparsulfatlösning och zink 15 p.
En blåfärgad vattenlösning av kopparsulfat reagerar med zink enligt följande reaktionsformel:
CuSO₄(aq) + Zn(s) → Cu(s) + ZnSO₄(aq)
3.1
I ett experiment var kopparsulfatlösningens volym 200,0 ml och koncentration 0,683 mol/l. Den metalliska zinkens massa var 1,85 g. Vi antar att reaktionen sker fullständigt. Hur många gram koppar kan bildas i experimentet?
Experimentet gav 1,066 g koppar. Beräkna det procentuella utbytet av koppar.
9 p.
n(CuSO₄) = c · V = 0,683 mol/l · 0,2000 l = 0,1366 mol
n(Zn) = m/M = 1,85 g/(65,38 g/mol) = 0,028296 mol
(1 p.)
Zinken tar slut i reaktionen eftersom substansmängden zink är mindre än substansmängden kopparsulfat, och de har samma koefficienter i reaktionsformeln.
(2 p.)
Utifrån koefficienterna i reaktionsformeln gäller att substansmängden koppar som bildas är n(Cu) = n(Zn)
(1 p.)
m(Cu) = n · M = 0,028296 mol · 63,55 g/mol = 1,7982 g
(1 p.)
Det bildas 1,80 g koppar.
(1 p.)
Utbytesprocenten för koppar = 1,066 g / 1,7982 g = 0,59281
(2 p.)
Utbytesprocenten för koppar var 59,3 % (0,593).
(1 p.)
3.2 Vilka observationer kan du göra under reaktionen? Nämn tre observationer som har att göra med reaktionen. 3 p.
1 p./observation, till exempel:
- Den gråfärgade metallen/zinken fräts.
- (Kopparsulfat)lösningens (blå) färg blir lite blekare.
- Det bildas rödaktig metall/koppar på ytan av den gråfärgade metallen/zinken och på botten av kärlet.
3.3 Är reaktionen en reduktions-oxidationsreaktion (redoxreaktion)? Motivera ditt svar med hjälp av oxidationstalen (oxidationstillstånden). 3 p.
Oxidationstalen för ämnena som reagerar:
| utgångsämne | produkt | |
|---|---|---|
| Cu | +2 | 0 |
| Zn | 0 | +2 |
(2 p.)
Eftersom oxidationstalen för de reagerande ämnena förändras är det fråga om en reduktions-oxidationsreaktion/redoxreaktion. (1 p.)
4. Syntes av fingolimod 15 p.
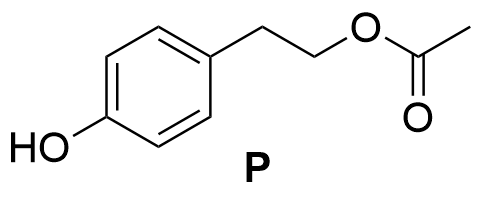
4.1 I det första steget av syntesen används en metod där endast den primära hydroxigruppen i förening O reagerar med ättiksyra. Då bildas mellanprodukten P som är en ester. Rita strukturformeln för mellanprodukt P. Du kan utnyttja fil i ditt svar. 3 p.
4.2 Fingolimod (Q) har följande sammansättning i massprocent: 74,22 % kol, 10,82 % väte, 4,556 % kväve och 10,41 % syre. Hur många kolatomer finns det i den kolvätekedja som i strukturformeln för fingolimod betecknas med bokstaven R? 7 p.
Uppgiften kan lösas på flera olika sätt. Nedan beskrivs ett av de här sätten.
Vi antar att vi har 100 g fingolimod. Då är
m(N) = 4,556 g, m(C) = 74,22 g, m(H) = 10,82 g och m(O) = 10,41 g.
(1 p.)
Då har vi följande substansmängder:
n(N) = m(N) / M(N) = 4,556 g / 14,01 g/mol = 0,325196 mol
n(C) = m(C) / M(C) = 74,22 g / 12,01 g/mol = 6,17985 mol
n(H) = m(H) / M(H) = 10,82 g / 1,008 g/mol = 10,734127 mol
n(O) = m(O) / M(O) = 10,41 g / 16,00 g/mol = 0,650625 mol
(2 p.)
Vi bestämmer den empiriska formeln för fingolimod:
N: 1
C: n(C) / n(N) = 6,17985 mol / 0,325196 mol = 19,0034 ≈ 19
H: n(H) / n(N) = 10,73413 mol / 0,325196 mol = 33,0081 ≈ 33
O: n(O) / n(N) = 0,650625 mol / 0,325196 mol = 2,00071 ≈ 2
(C₁₉H₃₃NO₂)ₓ
(1 p.)
Eftersom kedjan består av bara kol och väte finns det bara en kväveatom i fingolimod. Det här innebär att molekylformeln för fingolimod är C₁₉H₃₃NO₂.
(1 p.)
Utifrån strukturformeln för Q finns det 11 kolatomer i molekylen utöver de kolatomer som finns i kedjan R.
(1 p.)
Nu kan vi beräkna antalet kolatomer i kedjan R:
19 − 11 = 8.
(1 p.)
4.3 Hur skiljer sig vattenlösligheten för fingolimod (Q) vid pH-värdet 1 från dess vattenlöslighet vid pH-värdet 13? Motivera ditt svar. 5 p.
Vid pH-värdet 1 är vattenlösningen kraftigt sur. Då har aminogruppen i fingolimod tagit emot en proton / vätejon, så den är i sin syraform (-\mathrm{NH_3^+}). På motsvarande sätt är vattenlösningen kraftigt basisk vid pH-värdet 13. Då är aminogruppen i fingolimod i sin basform (-\mathrm{NH_2}), vilket innebär att den inte har mottagit eller avgivit en proton / vätejon. (2 p.)
En vattenmolekyl kan bilda jon-dipolbindningar med den positivt laddade aminogruppen (alltså med syraformen). Vattenmolekylen bildar vätebindningar med aminogruppen (alltså basformen), som enbart har delladdningar. Jon-dipolbindningarna är starkare än vätebindningarna. (2 p.)
Därför löser sig fingolimod bättre i en sur än i en basisk vattenlösning. (1 p.)
5. Bestämning av renheten hos ammoniumklorid 15 p.
5.1 Skriv alla reaktionsformler (reaktionslikheter) som hör ihop med det här experimentet. 6 p.
Reaktionen mellan ammoniumklorid och natriumhydroxid vid kokning:
NH₄Cl(s/aq) + NaOH(aq) → NH₃(g/aq) + NaCl(aq) + H₂O(l)
(2 p.)
Reaktionen mellan den frigjorda ammoniaken och vätekloridlösningen:
\mathrm{NH_3(g/aq)+HCl(aq)}\rightarrow\mathrm{NH_4^+(aq)+Cl^-(aq)}
(2 p.)
Reaktionen då vätekloridsyran titrerades med natriumhydroxid:
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
(2 p.)
5.2 Beräkna ammoniumkloridens renhet som massprocent. 7 p.
Den totala substansmängden väteklorid:
n(HCl)tot. = c · V = 0,100 l · 0,1013 mol/l = 10,130 · 10⁻³ mol
(1 p.)
Substansmängden väteklorid som titrerades:
n(HCl)översk. = n(NaOH)titr. = c · V = 0,1925 mol/l · 0,00712 l = 1,3706 ·10⁻³ mol
(1 p.)
Substansmängden ammoniumklorid:
n(NH₄Cl) = n(HCl)tot. − n(HCl)översk. = 10,130 · 10⁻³ mol − 1,3706 ·10⁻³ mol = 8,7594 ·10⁻³ mol
(2 p.)
Ammoniumkloridens massa och renhet:
m(NH₄Cl) = n · M = 8,7594 ·10⁻³ mol · 53,492 g/mol = 0,468558 g
(1 p.)
Renheten i massprocent = m(NH₄Cl)/m(prov) · 100 % = 0,46856 g / 0,5086 · 100 % = 92,12698 % = 92,1 %
(2 p.)
5.3 Varför var det viktigt att reaktionerna utfördes i ett dragskåp? 2 p.
I reaktionen frigörs ammoniakgas som har en stark lukt och som är kraftigt irriterande vid inandning. Även om ammoniaken tas upp av den sura vattenlösningen är det nödvändigt att försäkra sig om att ammoniaken inte i något skede kan hamna i inandningsluften.
6. Indigokarmin 15 p.
6.1 Vi ser närmare på indigokarminets form A. I molekylens ändar finns natriumsulfonatgrupper –SO₃Na. Namnge de övriga funktionella grupperna i indigokarminets form A. 4 p.
De rätta grupperna 1 p./grupp, högst 4 p.:
- aminogrupp
- hydroxigrupp
- karbonylgrupp
- dubbelbindning mellan kolatomer
- aromatisk ring / fenylgrupp
6.2 Vilken av indigokarminformerna A, B och C är mest oxiderad? Motivera ditt svar med hjälp av strukturen för indigokarmin. 4 p.
Den mest oxiderade formen är B. (2 p.)
Exempel på motivering: I form B är den relativa andelen syre i föreningen som högst. (2 p.)
6.3 I video hälls vattenlösningen över i ett annat dekanterglas och då oxideras indigokarminet. Vad är det som orsakar oxideringen av indigokarminet? Svaret behöver inte motiveras. 2 p.
Syret i luften orsakar oxidering av indigokarminet.
6.4 Förutom att hälla över vattenlösningen i ett annat dekanterglas, på vilket annat sätt skulle du kunna oxidera indigokarminet i vattenlösningen? Nämn ett sätt. 2 p.
Ett sätt ska nämnas i svaret. Till exempel kan det vara något av följande:
- Man kan röra om eller skaka lösningen.
- Man kan leda in syre i lösningen.
- Man kan tillsätta ett oxidationsmedel / ett oxiderande ämne till lösningen.
6.5 Glukos får indigokarmin att reduceras. Strukturformeln för glukos visas invid. Varför kan glukos fungera som ett reduktionsmedel? Motivera ditt svar med hjälp av strukturen för glukosmolekylen. 3 p.
I glukosen finns funktionella grupper som kan oxideras och samtidigt reducera indigokarminet. (1 p.)
Exempel på sådana grupper:
- En (primär) hydroxigrupp kan oxideras till en aldehyd.
- En (sekundär) hydroxigrupp kan oxideras till en keton.
- Aldehydgruppen kan oxideras till en karboxylsyra.
(2 p.)
7. Kvävetrikloridens jämvikt 15 p.
Kvävetriklorid NCl₃ är en förening som exploderar mycket lätt. I ett slutet kärl uppstår en jämvikt mellan kvävetriklorid och dess sönderfallsprodukter enligt följande:
2NCl₃(g) ⇌ N₂(g) + 3Cl₂(g)
Reaktionens jämviktskonstant är 3,3 · 10⁻¹² (mol²/l²).
7.1 En okänd mängd gasformig kvävetriklorid inneslöts i ett kärl som hade volymen 2,0 l. När jämviktsläget hade uppnåtts mätte man kvävets koncentration i kärlet, som var 3,2 · 10⁻⁶ mol/l. Hur många milligram kvävetriklorid hade ursprungligen inneslutits i kärlet? 8 p.
c = 3,2 · 10⁻⁶ mol/l
K = 3,3 · 10⁻¹²
M(NCl₃) = 14,01 g/mol + 3 · 35,45 g/mol = 120,36 g/mol
V = 2,0 l
Jämviktssituationen:
| 2NCl₃(g) | ⇌ | N₂(g) | + | 3Cl₂(g) | |
|---|---|---|---|---|---|
| I början | x | 0 | 0 | ||
| Förändring | −2c | +c | +3c | ||
| Vid jämvikt | x − 2c | c | 3c |
(2 p.)
K = [N₂][Cl₂]³ / [NCl₃]²
(1 p.)
= c · (3 · c)³ / (x − 2c)²
(1 p.)
Vi löser ut x:
x = \pm\sqrt{\frac{27c^4}{K}} + 2c
= 3,569037 · 10⁻⁵ mol/l (eller x = −2,289037 · 10⁻⁵ mol/l)
(1 p.)
Vi bestämmer massan för kvävetrikloriden i början:
n = x · V
m = n · M(NCl₃) = x · V · M(NCl₃) = 3,569037 · 10⁻⁵ mol/l · 2,0 l · 120,36 g/mol
= 0,008591386 g
= 8,6 mg
(3 p.)
7.2 I ett slutet kärl är kvävetrikloridens sönderfallsreaktion en jämviktsreaktion. Varför går reaktionen i ett öppet kärl bara i en riktning? 3 p.
I ett öppet utrymme kan produkterna spridas i omgivningen. (1 p.)
Därför kan inte sönderfallsreaktionens omvända reaktion ske i någon betydande grad (1 p.) och systemet uppnår inte ett jämviktstillstånd. (1 p.)
ELLER
I ett öppet utrymme kan produkterna spridas i omgivningen. (1 p.)
Produkter på den högra sidan av reaktionsformeln avgår (1 p.) och då förskjuts jämviktsläget fortgående mot produkterna och reaktionen uppnår aldrig ett jämviktstillstånd. (1 p.)
7.3 Bildningsentalpin för kvävetriklorid är 232 kJ/mol. Hur inverkar en höjning av temperaturen på jämviktsläget för kvävetrikloridens sönderfallsreaktion? Motivera ditt svar. 4 p.
Kvävetrikloridens sönderfallsreaktion är den omvända reaktionen till dess bildningsreaktion. Därmed är reaktionsentalpin för den omvända reaktionen det motsatta talet till bildningsentalpin, alltså −232 kJ/mol. (2 p.)
Sönderfallsreaktionen är alltså exoterm. (1 p.)
Därför förskjuts jämviktsläget mot utgångsämnena när temperaturen höjs. (1 p.)
8. Kolvätens orbitaler 15 p.
8.1
Välj rätt hybridisering. Rätt svar 1 p., fel svar 0 p., inget svar 0 p.
Om du har börjat besvara uppgiften men kommer till att du ändå inte vill lämna in den för bedömning kan du radera ditt svar genom att välja den tomma raden i rullgardinsmenyn.
3 p.
8.1.1 Vilken är kolatomernas hybridisering i etan? 1 p.
- sp³ (1 p.)
8.1.2 Vilken är kolatomernas hybridisering i eten? 1 p.
- sp² (1 p.)
8.1.3 Vilken är kolatomernas hybridisering i etyn? 1 p.
- sp (1 p.)
8.2 Förekommer det konformationsisomeri för eten H₂C=CH₂? Motivera ditt svar med hjälp av orbitalerna. 5 p.
(I eten är kolatomerna sp²-hybridiserade.) Två sp²-hybridorbitaler samt två p-orbitaler, vilka är vinkelräta mot molekylens plan, deltar i bildandet av C–C-bindningen. (1 p.)
De här orbitalerna bildar en σ-bindning och en π-bindning. (1 p.)
π-bindningen kan inte vridas fritt. Det här hindrar att CH₂-grupperna skulle vridas fritt runt C=C-dubbelbindningen. (2 p.)
Därför förekommer det inte konformationsisomeri hos eten. (1 p.)
8.3 Strukturformeln för bensoesyra visas invid. I bensoesyran har alla kolatomerna hybridiseringen sp². Vilka slutsatser kan du utifrån det här dra gällande bensoesyrans tredimensionella struktur? Motivera ditt svar. 3 p.
De sp²-hybridiserade kolatomerna utgör en plan struktur. Vi kan därmed dra slutsatsen att bensenringen är plan. Kolatomen i karboxylsyragruppen, de två syreatomerna och kolatomen i bensenringen som binder till karboxylsyragruppen är alla sinsemellan i samma plan. Vi kan ändå inte utifrån en analys av kolatomernas hybridisering avgöra i vilken riktning väteatomen i hydroxigruppen är riktad.
8.4 Motivera med hjälp av orbitalstrukturen för bensen varför alla dess sex kol-kolbindningar är lika långa. 4 p.
(Kolatomerna är sp²-hybridiserade.) Det finns en likadan σ-bindning mellan varje kolatom och dess bredvidliggande kolatom. (1 p.)
De sex p-orbitalerna som är riktade vinkelrätt mot molekylens plan förenas (1 p.)
och då bildas en π-bindning som är delokaliserad runt hela ringen. (2 p.)
(Därmed är alla kol-kolbindningar identiska.)
Del 3: 20-poängsuppgifter
9. Framställning av tellur 20 p.
Tellur är en silvergrå halvmetall som används bland annat i solceller. Dess kemiska egenskaper liknar svavlets.
Tellur förekommer bland annat i kopparmalm som koppar(I)tellurid Cu₂Te. När koppar förädlas ansamlas koppar(I)tellurid i det slam som bildas som biprodukt under elektrolysen av koppar. Tellur framställs ur den här biprodukten genom en process med flera steg.
9.1
I det första steget av separationsprocessen för tellur hettar man upp koppar(I)tellurid tillsammans med natriumkarbonat vid 500 ℃. Koppar(I)telluriden reagerar med natriumkarbonatet och luftens syre, och då bildas natriumtellurit Na₂TeO₃ i fast form och metalliskt koppar. I reaktionen frigörs koldioxid.
Skriv reaktionsformeln (reaktionslikheten) som beskriver det här steget i processen.
3 p.
Cu₂Te(s) + O₂(g) + Na₂CO₃(s) → Na₂TeO₃(s) + 2Cu(s) + CO₂(g)
- Alla ämnen är rätt. (1 p.)
- Därtill är alla koefficienter rätt (1 p.) och alla aggregationstillstånd är rätt (1 p.).
9.2 Vilka miljöpåverkningar har processen som beskrivs i deluppgift 9.1? Nämn tre exempel. 3 p.
I svaret beskrivs till exempel tre av följande (1 p./exempel):
- Den relativt höga temperaturen kräver energi. Miljöeffekterna beror på vilken energikälla som används. Om energin till exempel produceras med fossila bränslen, ger det här upphov till koldioxidutsläpp.
- Koldioxiden som bildas som produkt är en växthusgas.
- Produktionen av natriumkarbonatet som används som utgångsämne konsumerar energi och råvaror.
- Tellurföreningarna (som är i någon mån giftiga) måste omsorgsfullt tas om hand i processen. De får inte släppas ut i naturen.
9.3
I följande steg av separationsprocessen löser man upp natriumtelluriten Na₂TeO₃ i vatten och då separeras natriumtelluriten från den metalliska kopparn.
Telluritjonen \mathrm{TeO}_3^{2-} är en bas. Dess konjugerade syra är vätetelluritjonen \mathrm{HTeO}_3^{-}, vars syrakonstant har värdet 2,3 · 10⁻³ (mol/l).
Skriv reaktionsformeln (reaktionslikheten) för telluritjonens protonöverföringsreaktion.
4 p.
\mathrm{TeO_3^{2-}(aq)}+\mathrm{H_2O(l)}\xrightleftharpoons{ }\ \mathrm{HTeO_3^-(aq)}+\mathrm{OH^-(aq)}
ELLER
Na₂TeO₃(aq) + H₂O(l) ⇌ NaHTeO₃(aq) + NaOH(aq)
- Alla ämnen är rätt. (1 p.)
- Därtill är alla koefficienter rätt (2 p.) och alla aggregationstillstånd är rätt (1 p.).
9.4
I det därpå följande steget av separationsprocessen tillsätts svavelsyra till vattenlösningen av natriumvätetellurit. Då faller tellurdioxid TeO₂ ut ur lösningen:
2NaHTeO₃(aq) + H₂SO₄(aq) → 2TeO₂(s) + Na₂SO₄(aq) + 2H₂O(l)
Tellurdioxiden TeO₂ kan på elektrolytisk väg reduceras ur en sur vattenlösning till tellur.
Skriv reaktionsformlerna (reaktionslikheterna) för anod- och katodreaktionerna samt totalreaktionen för den elektrolytiska reduktionen av tellurdioxid. Antag att elektroderna är inerta. I den här deluppgiften behöver du inte skriva ut aggregationstillstånd i reaktionsformlerna.
6 p.Anoden:
2H₂O → O₂ + 4H⁺ + 4e⁻
(2 p.)
Katoden:
TeO₂ + 4H⁺ + 4e⁻ → Te + 2H₂O
(2 p.)
Totalreaktionen:
TeO₂ → Te + O₂
(2 p.)
9.5
I stället för att använda elektrolys enligt beskrivningen i deluppgift 9.4 kan man också reducera tellurdioxiden med en reaktion i vilken svaveldioxid i gasform leds in i en blandning bestående av tellurdioxid och svavelsyra:
TeO₂(s) + 2SO₂(g) + 2H₂O(l) → Te(s) + 2H₂SO₄(aq)
Vi ser närmare både på reduktionsprocessen som utgår från svaveldioxid och på reduktionsprocessen som utgår från elektrolys, vilken beskrivs i deluppgift 9.4. Vad borde man beakta i de här processerna för att framställningen av tellur ska vara så miljövänlig som möjligt?
4 p.Reduktion på elektrolytisk väg, 1 p. /aspekt, högst 2 p. Exempel på olika aspekter:
- Elektrolysen kräver en stor mängd elenergi och denna bör produceras med förnybara energikällor för att minimera miljöpåverkan.
- (Tellur är i någon mån giftigt.) Telluren måste omsorgsfullt tas om hand i processen. Den får inte släppas ut i miljön.
Reduktion med svaveldioxid, 1 p. /aspekt, högst 3 p. Exempel på olika aspekter:
- Produktionen av svaveldioxid konsumerar energi.
- Svaveldioxid i gasform får inte släppas ut i miljön.
- En vattenlösning av svaveldioxid är frätande och skadlig för vattenlevande organismer, så den får inte släppas ut i miljön.
- Man måste kunna ta hand om och återanvända svavelsyran som bildas som en biprodukt.
10. Reaktionshastighet och aktiveringsenergi 20 p.
10.1 Är reaktionen mellan brommetan och hydroxidjonen, som beskrivs i graf , exoterm eller endoterm? Motivera ditt svar. 3 p.
Reaktionen är exoterm. (1 p.)
Det frigörs energi i reaktionen för att utgångsämnenas energi är högre än produkternas (eller produkternas energi är lägre än utgångsämnenas). (2 p.)
10.2 Hur skulle en katalysator inverka på förloppet av den reaktion som beskrivs i graf ? Ge svaret som en bild. Ta en skärmdump av graf eller spara grafen som en bild. Använd ett ritprogram och komplettera grafen med tillägg som beskriver hur reaktionen framskrider när man använder katalysator. Ta en skärmdump av den kompletterade bilden som du producerat och bifoga skärmdumpen till svaret. 4 p.
Följande ska framgå ur bilden:
- Energierna för utgångsämnena och produkterna är desamma oavsett om man använder katalysator eller inte. (2 p.)
- Reaktionens aktiveringsenergi är lägre när man använder en katalysator jämfört med den ursprungliga reaktionen utan katalysator. (2 p.)
Till exempel:
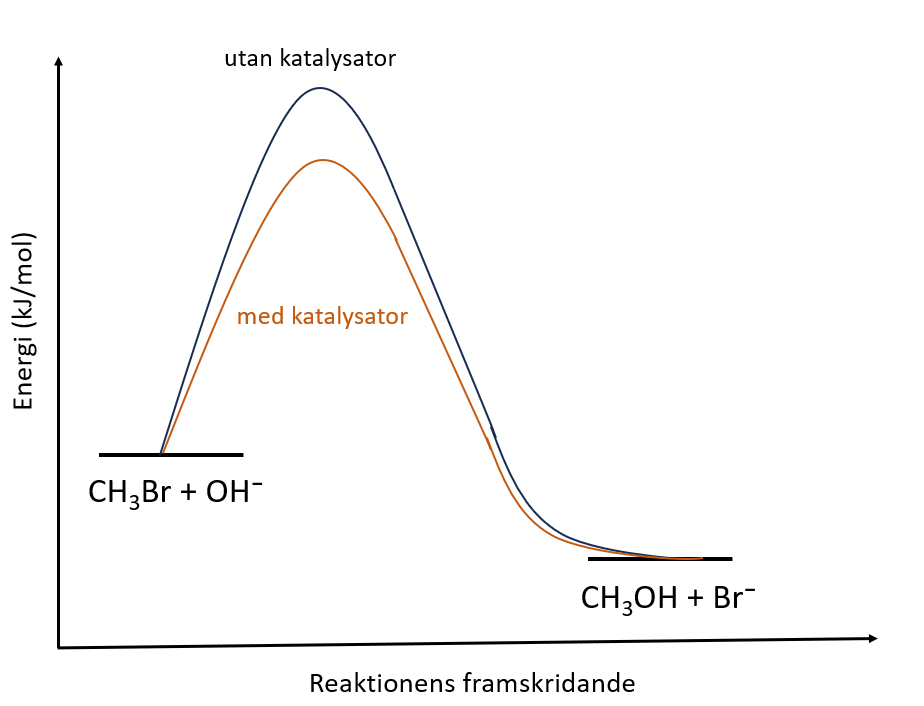 Exempel på bild som ges i svaret.
Exempel på bild som ges i svaret.
10.3 Metanol kan produceras i en reaktion mellan koldioxid och väte. På industriell skala effektiviserar man reaktionen genom att införa en katalysator i reaktionskammaren. Planera en undersökning för att utreda hur två olika katalysatorer inverkar på reaktionshastigheten. Beskriv hur undersökningen utförs, vilka mätningar som görs och vilka faktorer som hålls konstanta. 5 p.
Man utför två separata experiment. I det ena experimentet används katalysatorn A och i det andra experimentet används katalysatorn B. I vardera experimentet mäter man förändringarna i koncentrationen för antingen någondera utgångsämnet eller för produkten. (2 p.)
I vardera experimentet mäts förändringen efter samma tidsperiod. (1 p.)
Temperaturen och koncentrationerna/(del)trycken för utgångsämnena ska vara lika stora i början av båda experimenten. (2 p.)
10.4
Aktiveringsenergin för sönderfallsreaktionen för vätejodid (2HI → H₂ + I₂) är 179 kJ/mol. Vid temperaturen 573 K har den naturliga logaritmen av reaktionens hastighetskoefficient värdet ln(k) = −12,747. Vilket ska värdet för aktiveringsenergin vara för att reaktionens hastighetskoefficient ska fördubblas vid temperaturen 573 K?
ln(2k) = −12,054
8 p.
Vi gör följande beteckningar: Aktiveringsenergin Eₐ₁ motsvarar hastighetskoefficienten k₁ och aktiveringsenergin Eₐ₂ motsvarar hastighetskoefficienten k₂.
ln(k₁) = ln(A) − Eₐ₁/(RT)
ln(k₂) = ln(2k₁) = ln(A) − Eₐ₂/(RT)
(2 p.)
ln(k₁) − ln(2k₁) = Eₐ₂/(RT) − Eₐ₁/(RT)
Eₐ₂/(RT) = ln(k₁) − ln(2k₁) + Eₐ₁/(RT)
(3 p.)
Eₐ₂ = RT(ln(k₁) − ln(2k₁)) + Eₐ₁
= 8,314463 J/(K mol) · 573 K (−12,747 − (−12,054)) + 179 000 J/mol
= 175 698,42 J/mol
= 176 kJ/mol
(3 p.)
11. Aminers reaktioner 20 p.
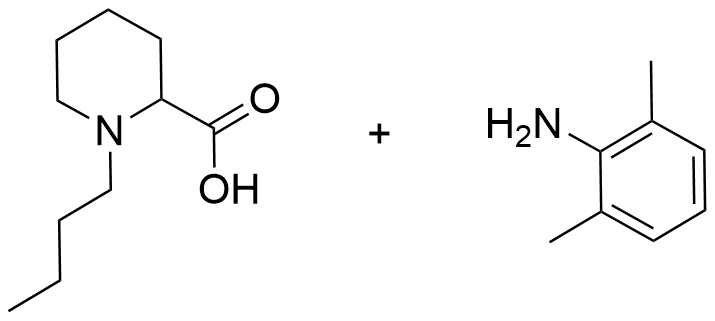
11.1 Rita strukturformlerna för produkterna som bildas i reaktion A . Du kan utnyttja strukturformeln för bupivakain i fil i ditt svar. 4 p.
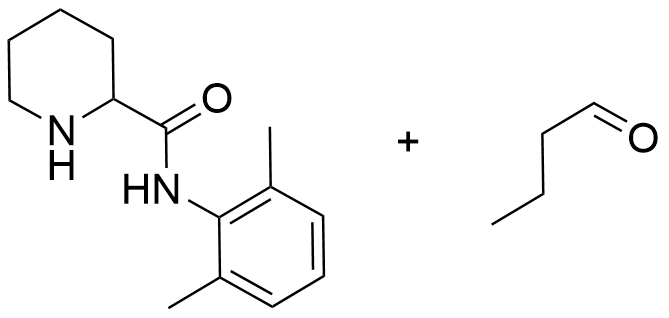
11.2 Rita strukturformlerna för produkterna som bildas i reaktion B. Du kan utnyttja strukturformeln för bupivakain i fil i ditt svar. 4 p.
11.3
När en viss gasformig amin (CxHyNz) förbrändes bildades produkterna koldioxid (CO2), kväve (N2) och vatten (H2O). Aminens förbränningsreaktion är:
2CxHyNz(g) + (4x + y)/2O2(g) → 2xCO2(g) + zN2(g) + yH2O(g).
Som utgångsämne i reaktionen användes 10,0 ml amin. När den resulterande gasblandningen kyldes ned till rumstemperatur hade 25,0 ml gas avgått från gasblandningen. Volymminskningen berodde på att aggregationstillståndet för en av reaktionsprodukterna hade förändrats. När gasblandningen sedan tvättades med en basisk tvättlösning avlägsnades 10,0 ml gas från gasblandningen. Efter tvätten fanns det slutligen 5,0 ml gas kvar. Alla volymer uppmättes vid rumstemperatur.
Använd den givna informationen för att bestämma koefficienterna x, y och z. Motivera ditt svar.
Skriv den balanserade reaktionsformeln (reaktionslikheten) i ditt svar och namnge den amin som var utgångsämne.
Luftfuktigheten och vattnets ångtryck beaktas inte. Alla gaser antas vara idealgaser. Volymen för en idealgas är direkt proportionell mot gasens substansmängd.
12 p.2CxHyNz(g) + (4x + y)/2O₂(g) → 2xCO₂(g) + zN₂(g) + yH₂O(g)
Eftersom reaktionen bara omfattade gaser kan de stökiometriska koefficienterna användas direkt för att ange sambandet mellan de reagerande ämnenas substansmängder eller mellan deras volymer.
Slutledningsprocessen för att bestämma koefficienten y:
När blandningen kyldes ned till rumstemperatur kondenserades vattenångan till vätska så den avgick från gasblandningen. Det fanns 25,0 ml vattenånga.
(1 p.)
När vi jämför mängden vattenånga med mängden amin ser vi att det fanns 25,0 ml/10 ml, alltså 2,5 gånger så mycket vatten som amin. Därmed är vattnets koefficient y = 2 · 2,5 = 5.
(2 p.)
Slutledningsprocessen för att bestämma koefficienten x:
I gasblandningen som blev kvar fanns det koldioxid och kväve. Koldioxiden avgick med den basiska tvättlösningen. Det fanns därmed 10,0 ml koldioxid.
(1 p.)
Vi ser att koefficienten x = 1, för det fanns 10 ml amin och det bildades 10 ml koldioxid.
(1 p.)
Nu kan vi bestämma syrets koefficient (4x + y)/2 = (4 · 1 + 5)/2 = 4,5.
(2 p.)
Slutledningsprocessen för att bestämma koefficienten z:
Efter tvätten fanns det bara kvävgas kvar (5,0 ml).
(1 p.)
Vi ser att koefficienten z = 1 för det fanns 10,0 ml amin som utgångsämne och det bildades 5 ml kväve.
(2 p.)
Nu har vi bestämt alla koefficienter i reaktionsformeln:
2CH₅N(g) + 4,5O₂(g) → 2CO₂(g) + N₂(g) + 5H₂O(g).
Vi måste ännu multiplicera koefficienterna med två för att koefficienten för syre ska bli ett heltal:
4CH₅N(g) + 9O₂(g) → 4CO₂(g) + 2N₂(g) + 10H₂O(g).
(1 p.)
Föreningen är metylamin/metanamin.
(1 p.)